题目内容
11.将125g含杂质(杂质不参加反应,也不溶于水)20%的大理石放到500g稀盐酸中,恰好完全反应.求:(1)所用稀盐酸的溶质的质量分数是多少?
(2)反应后所得溶液中溶质的质量分数是多少?(计算结果精确到0.1%)
分析 碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,根据提供的数据和反应的化学方程式可以进行相关方面的计算.
解答 解:(1)设稀盐酸中氯化氢质量为x,反应生成氯化钙的质量为y,生成二氧化碳质量为z,
大理石中碳酸钙质量为:125g×(1-20%)=100g,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 111 44
100g x y z
$\frac{100}{100g}$=$\frac{73}{x}$=$\frac{111}{y}$=$\frac{44}{z}$,
x=73g,y=111g,z=44g,
所用稀盐酸的溶质的质量分数是:$\frac{73g}{500g}$×100%=14.6%,
答:所用稀盐酸的溶质的质量分数是14.6%.
(2)反应后所得溶液中溶质的质量分数是:$\frac{111g}{100g+500g-44g}$×100%=20.0%,
答:反应后所得溶液中溶质的质量分数是20.0%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,同时考查了分析数据的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.合肥市第55届“元旦健身走”活动于2015年1月在渡江战役纪念馆外隆重举行,下列关于该纪念馆在修建过程中所需的材料在加工、制造过程中只发生物理变化的是( )
| A. | 玻璃 | B. | 钢材 | C. | 大理石 | D. | 高分子材料 |
20.下列对实验现象的描述正确的是( )
| A. | 向鸡蛋清溶液中加入饱和(NH4)2SO4溶液,生成白色固体 | |
| B. | 向淀粉中滴加加碘食盐溶液,溶液变蓝色 | |
| C. | 打开浓盐酸的瓶塞,瓶口出现白烟 | |
| D. | 将葡萄糖与碱性Cu(OH)2悬浊液混合,出现红色固体 |
1.如图所示的实验操作正确的是( )
| A. | 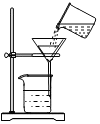 过滤 | B. | 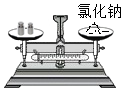 称量固体 称量固体 | C. | 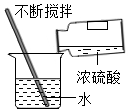 稀释浓硫酸 | D. | 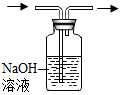 除去CO2中的CO |