题目内容
4.某温度下,100克饱和氯化钠溶液中含有26.5克氯化钠.若在该温度下向此溶液中加入3克氯化钠和7克水,则所得溶液中溶质的质量分数为( )| A. | $\frac{26.5g+3g}{100g+7g}$×100% | B. | 30% | ||
| C. | $\frac{26.5g+3g}{100g+7g+3g}$×100% | D. | 26.5% |
分析 100g饱和氯化钠溶液中含有26.5g氯化钠,含有水的质量为:100g-26.5g=73.5g,氯化钠和水的质量比为:26.5g:73.5g=53:147,3g:7g=63:147,因此7g水中不能完全溶解3g氯化钠,即在该温度下向此溶液中加入3g氯化钠和7g水时,得到的仍然是氯化钠的饱和溶液,只要温度不变,物质的饱和溶液的质量分数不变.
解答 解:100g饱和氯化钠溶液中含有26.5g氯化钠,含有水的质量为:100g-26.5g=73.5g,氯化钠和水的质量比为:26.5g:73.5g=53:147,3g:7g=63:147,因此7g水中不能完全溶解3g氯化钠,即在该温度下向此溶液中加入3g氯化钠和7g水时,得到的仍然是氯化钠的饱和溶液,所得溶液中溶质的质量分数为:
$\frac{26.5g}{100g}$×100%=26.5%,
故选:D.
点评 本题主要考查学生进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
12.烧杯中盛有一定质量、温度为60℃的KNO3溶液,将其置于室温环境中,测定不同温度时析出晶体的质量,测定结果记录如表.若不考虑水蒸发对实验的影响,请回答下列问题
(1)30℃时,该溶液是否为饱和溶液?是(选填“是”“否”或“无法判断”)
(2)在某一温度时,将接近饱和的KNO3溶液变成饱和溶液,下列方法中一定可行的是②③⑤(填序号)
①升温 ②降温 ③加溶质 ④加水 ⑤恒温蒸发水.
| 溶液的温度/℃ | 50 | 40 | 30 | 20 |
| 析出固体的质量/g | 0 | 0 | 2.0 | 8.4 |
(2)在某一温度时,将接近饱和的KNO3溶液变成饱和溶液,下列方法中一定可行的是②③⑤(填序号)
①升温 ②降温 ③加溶质 ④加水 ⑤恒温蒸发水.
9.工业制取硅的其中一步反应原理是SiCl4+2H2$\frac{\underline{\;高温\;}}{\;}$Si+4HCl,该反应属于基本反应类型中的( )
| A. | 化合反应 | B. | 分解反应 | C. | 置换反应 | D. | 复分解反应 |
16.重铬酸根在酸性条件下具有强氧化性,它的化学式:Cr2O72-,已知其中氧元素显-2价,由此可判断其中铬元素的化合价为( )
| A. | +8 | B. | +6 | C. | +5 | D. | +3 |
6.我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破.其成果在最近的美国《科学》杂志发表.该转化的微观示意图如图所示.有关说法正确的是( )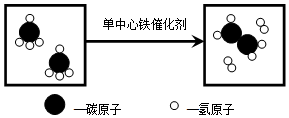

| A. | 该反应属于复分解反应 | B. | 单中心铁催化剂没有参与此反应 | ||
| C. | 生成物之一为H2 | D. | 反应物与生成物共有4种分子 |
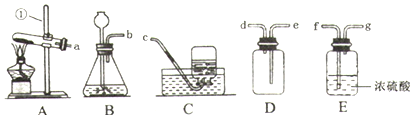
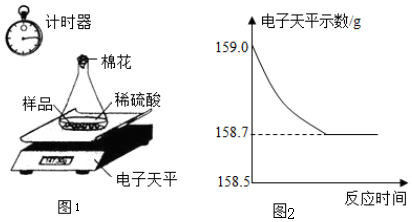

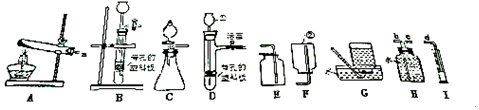
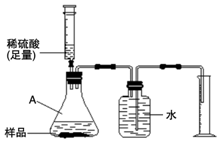 侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质.某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案
侯德榜是我国著名的化学家.由他发明的侯氏制碱法制得的纯碱中含有少量氯化钠杂质.某化学兴趣小组的同学为了测定该厂生产的纯碱是否属于优等品(国家规定:优等品中碳酸钠的质量分数不低于99.2%),设计了如下两种实验方案