题目内容
17.除去下列物质中的少量杂质(括号内的为杂质),方法合理的是( )| A. | CO2(CO):点燃 | |
| B. | KNO3(K2SO4):溶解,加过量的硝酸钡溶液 | |
| C. | CaCl2(CaCO3):加水溶解、过滤、蒸发 | |
| D. | 铁粉(Fe2O3):加适量稀盐酸,过滤 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、除去二氧化碳中的一氧化碳不能够点燃,这是因为会引入新的气体杂质,且当二氧化碳(不能燃烧、不能支持燃烧)大量存在时,少量的一氧化碳是不会燃烧的;故选项所采取的方法错误.
B、溶解后,过量的硝酸钡能与K2SO4液反应生成硫酸钡沉淀和硝酸钾,能除去杂质但引入了新的杂质硝酸钡(过量的),不符合除杂原则,故选项所采取的方法错误.
C、氯化钙易溶于水,碳酸钙难溶于水,可采取加水溶解、过滤、蒸发的方法进行分离除杂,故选项所采取的方法正确.
D、铁粉和Fe2O3均能与稀盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
故选:C.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
10.下列关于水的净化过程的描述错误的是( )
| A. | 加入明矾使小颗粒凝聚 | B. | 利用二氧化氯杀菌消毒 | ||
| C. | 通过沙滤装置除去可溶性杂质 | D. | 通过活性炭吸附部分有害物质 |
5.化学中常常出现“1+1≠2”的有趣现象,但也有例外,下列符合“1+1=.2”的事实是( )
| A. | 1L水与1L酒精混合后体积等于2L | |
| B. | lg镁和lg稀硫酸充分反应后所得的溶液质量为2g | |
| C. | lg硫粉在lg氧气中完全燃烧后生成2g二氧化硫 | |
| D. | lg镁在lg氧气中燃烧会得到2g氧化镁 |
12.中国古代的下列发明创造中,不涉及化学变化的是( )
| A. | 用胆矾炼铜 | B. | 用铁矿石炼铁 | ||
| C. | 用黏土烧制陶瓷 | D. | 打磨磁石制指南针 |
2.在一定条件下,将A、B、C、D四种物质放在密闭容器内反应一段时间,测得化学反应前后各物质的质量如表:
根据上表数据计算:
(1)该反应的反应物是B,生成物是CD;
(2)表中“x”值为5g;
(3)该反应属于分解反应(填“化合”或“分解”);
(4)B、C两种物质变化的质量比为7:1.
| 物质 | A | B | C | D |
| 反应前质量/g | 5 | 112 | 16 | 4 |
| 反应后质量/g | x | 0 | 32 | 100 |
(1)该反应的反应物是B,生成物是CD;
(2)表中“x”值为5g;
(3)该反应属于分解反应(填“化合”或“分解”);
(4)B、C两种物质变化的质量比为7:1.
6.高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等功能为一体的新型高效水处理剂,可将水中的三氯乙烯(C2HCl3)除去85.6%,下列说法正确的是( )
| A. | K2FeO4中Fe元素的化合价为+3价 | |
| B. | K2FeO4的相对分子质量为198 | |
| C. | C2HCl3中碳、氢、氯三种元素质量比是2:1:3 | |
| D. | C2HCl3表示三氯乙烯由2个碳原子、1个氢原子和3个氯原子构成 |
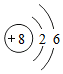 氧是地壳中含量最多的元素,氧及其化合物是化学学习和研究的重要内容.
氧是地壳中含量最多的元素,氧及其化合物是化学学习和研究的重要内容.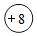 表示原子核,带8个单位正电荷
表示原子核,带8个单位正电荷