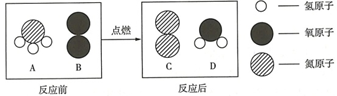
题目内容
2.100g溶质质量分数为4.9%的稀硫酸与一定质量一定质量分数的氢氧化钠溶液正好完全反应,测得反应后溶液的质量为200g.求:(1)该氢氧化钠溶液的溶质质量分数;
(2)反应后所得溶液的溶质质量分数.
分析 硫酸与氢氧化钠溶液反应生成硫酸钠和水;由参加反应的稀硫酸的质量、溶质的质量分数,由反应的化学方程式列式计算出参加反应的氢氧化钠的质量、生成硫酸钠的质量,进而计算出氢氧化钠溶液的溶质质量分数、反应后所得溶液的溶质质量分数即可.
解答 解:设参加反应的氢氧化钠的质量为x,生成硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 98 142
x 100g×4.9% y
$\frac{80}{98}=\frac{x}{100g×4.9%}$ x=4g.
$\frac{98}{142}=\frac{100g×4.9%}{y}$ y=7.1g.
(1)该氢氧化钠溶液的溶质质量分数为$\frac{4g}{200g-100g}×$100%=4%;
(2)反应后所得溶液的溶质质量分数为$\frac{7.1g}{200g}$×100%=3.55%.
答:(1)该氢氧化钠溶液的溶质质量分数为4%;
(2)反应后所得溶液的溶质质量分数为3.55%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
10.下列各项为小明同学记录的物质燃烧现象,与事实相符的是( )
| A. | 铁丝在氧气中燃烧时,发耀眼的白光 | |
| B. | 硫粉在氧气中燃烧时,产生蓝紫色火焰 | |
| C. | 木炭在空气中燃烧时,发出白光 | |
| D. | 红磷在空气中燃烧时,冒出大量的白雾 |
17.碱式碳酸铜受热分解生成CuO、CO2和H2O三种物质,则碱式碳酸铜的组成是( )
| A. | 一定含有碳、氢、铜元素,可能含有氧元素 | |
| B. | 肯定有碳、氢、氧、铜四种元素 | |
| C. | 一定含有碳、氢、氧元素,可能含有铜元素 | |
| D. | 只含有碳、氢、氧元素 |
4.规范的实验操作是实验成功的必要条件.下列实验操作中,不正确的是( )
| A. |  加热液体 | B. | 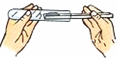 取用粉末固体 | C. | 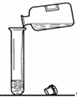 取用液体药品 | D. | 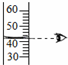 读液体体积 |
5.下列化学符号中的数字“2”表示的意义,正确的是( )
| A. | $\stackrel{+2}{Ca}$:氧化钙中钙元素的化台价为+2价 | |
| B. | 2O:2个氧元素 | |
| C. | Mg2+:两个镁离子 | |
| D. | N2:2个氮分子 |