题目内容
2.下列事实能说明粒子之间有间隔的是( )| A. | 热胀冷缩 | B. | 美酒飘香 | C. | 水果腐烂 | D. | 糖甜醋酸 |
分析 根据微观粒子的基本特征:粒子质量和体积都很小;粒子之间有间隔;粒子是在不断运动的;同种物质的粒子性质相同,不同物质的粒子性质不同,结合事实进行分析判断即可.
解答 解:A、热胀冷缩是因为粒子间的间隔受热时增大,遇冷时缩小的缘故,说明分子之间有间隔;
B、美酒飘香是因为美酒中含有的分子不断运动,向四周扩散,使人们闻到酒的香气;
C、水果腐烂是由于分子本身发生了改变;
D、盐咸糖甜说明不同物质的粒子性质不同.
故选A.
点评 本题难度不大,掌握微观粒子的基本性质及利用粒子的基本性质分析和解决问题的方法是解答此类题的关键.

练习册系列答案
相关题目
12.工业上常利用电石制乙炔气体(C2H2)时产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如图:
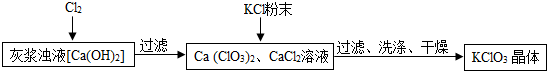
(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
上述流程中加入KCl粉末,KCl与Ca(ClO3)2(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3 晶体的原因是KClO3在常温下溶解度较小.
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
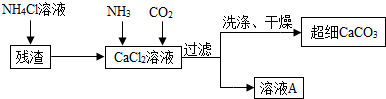
(5)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.检验CaCO3是否洗涤干净的方法是取最后一次的洗涤液加硝酸银溶液,如有沉淀生成则没有洗干净,反之以洗干净.
(6)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,写出该反应的化学方程式CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如图:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Cl2+6Ca(OH)2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):

(5)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+2NH3+CO2+H2O=CaCO3↓+2NH4Cl.检验CaCO3是否洗涤干净的方法是取最后一次的洗涤液加硝酸银溶液,如有沉淀生成则没有洗干净,反之以洗干净.
(6)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
11.20℃时,将某物质的溶液分成质量相等的两份,其中一份蒸发10g水达到饱和,其二加入3.4g该物质也能达到饱和,20℃时,对该物质的结论正确的是( )
| A. | 溶解度为34g | |
| B. | 是一种易溶物 | |
| C. | 溶质质量分数的最大值为30% | |
| D. | 若要使20℃时饱和溶液的质量分数增大一倍,可采用蒸发溶剂的方法 |
19.某反应的微观示意图如图,下列说法正确的是( )
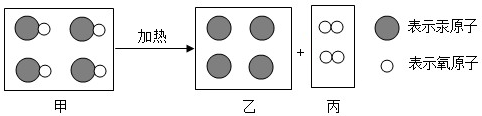

| A. | 图中甲、乙、丙三种物质均是由分子构成的 | |
| B. | 图中甲、乙、丙三种物质中,乙、丙属于单质 | |
| C. | 该反应前后分子种类、原子种类均没有改变 | |
| D. | 该反应是化合反应 |
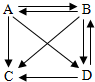 某同学画出的四种物质之间的转化关系图,A、B、C、D代表最常见的含有钠离子的四种物质的溶液,“→”表物质间的转化关系,所有的转化关系都可以通过复分解反应实现.钠离子的符号是Na+,C中溶质的化学式NaNO3 .写出A→B的化学方程式2NaOH+CO2═Na2CO3+H2O;写出D→C的化学方程式NaCl+AgNO3═AgCl↓+NaNO3 .
某同学画出的四种物质之间的转化关系图,A、B、C、D代表最常见的含有钠离子的四种物质的溶液,“→”表物质间的转化关系,所有的转化关系都可以通过复分解反应实现.钠离子的符号是Na+,C中溶质的化学式NaNO3 .写出A→B的化学方程式2NaOH+CO2═Na2CO3+H2O;写出D→C的化学方程式NaCl+AgNO3═AgCl↓+NaNO3 .