��Ŀ����
8���������ƣ�NaN3�����㷺Ӧ����������ȫ���ң�ij��ѧС��ͬѧ������������о���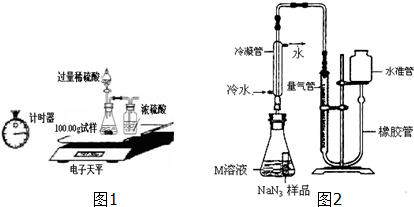
���������ϡ�
��NaN3��ײ����Ѹ�ٷֽ�����Na��N2��д���÷�Ӧ�Ļ�ѧ����ʽ2NaN3$\frac{\underline{\;ײ��\;}}{\;}$2Na+3N2����
��NaN3�����ᡢH2SO4��Һ���������ɣ�
�ۼ�ʯ����CaO�� NaOH�Ļ���
��NaN3��ҵ���Ʊ������ǣ�����������Һ̬����Ӧ�Ƶ�NaNH2���ٽ�NaNH2��N2O��Ӧ������NaN3��NaOH������X���÷�Ӧ�Ļ�ѧ����ʽΪ2NaNH2+N2O=NaN3+NaOH+X����X�Ļ�ѧʽΪNH3��
������̽����
��һ���ⶨij��ҵ��NaN3��Ʒ��Na2CO3����������
��1����ҵ��NaN3�г�����������Na2CO3����ԭ���ǣ��û�ѧ����ʽ��ʾ��2NaOH+CO2�TNa2CO3+H2O��
��2��ijͬѧ�����ͼ1װ�ò��̼���Ƶ�������������ʵ�����ݼ�¼���£�
| ������Ŀ | ����ʱ�� | ������g�� |
| ���� | 100.00 | |
| װ��+ϡ�������� | 241.20 | |
| װ��+ϡ��������+���� | ��Ӧ��ʼ��15�� | 339.20 |
| װ��+ϡ��������+���� | ��Ӧ��ʼ��35�� | 339.00 |
| װ��+ϡ��������+���� | ��Ӧ��ʼ��55�� | 339.00 |
������Ũ�����ϴ��װ�ã���ʹ�ⶨ�Ľ��ƫ���ƫ����ƫС�����䡱����
�����ñ������ݼ����̼���Ƶ���������Ϊ5.3%��
������̽����
�������ⶨij��ҵ����Ʒ��NaN3����������
С̸ͬѧ��ȷ����0.140g NaN3��Ʒ�������ͼ2װ�òⶨ������������
��֪2NaN3��3N2��NaN3�е�Nȫ��ת��ΪN2�����������ԣ�����Ӧ�зų��������ȣ�
��1������װ�������Եķ����ǣ����Ӻ�װ�ã���ˮ��עˮ���������߳����ȶ���Һ��˵�����������ã�
��2��ʹ����ˮ������Ŀ���ǣ�ʹˮ����Һ����
��3����б��ƿʹС�Թ��е�NaN3��Ʒ��M��Һ�Ӵ���ַ�Ӧ�� �����²�������ܶ���Ϊ67.2mL��N2���ܶ�Ϊ1.25g/L������ʵ����ѡ�õ������ܹ����ʵ���A������ĸ��ţ���
A.100mL B.1L C.2L
��4�����㹤ҵ����Ʒ��NaN3������������д��������̣��������0.1%����
���� ���������ϡ���
�ٸ�����Ϣ�жϷ�Ӧ��������Ӧ������Ȼ��д������ʽ��
�ܸ��������غ㶨�ɵ�ʵ�����ж�X�Ļ�ѧʽ���ٸ������������Կ��ǣ�
������̽������
��һ��
��1���������ƺͿ����еĶ�����̼��Ӧ��Ӧ����̼���ƣ��ݴ˻ش�
��2���ٴ���Ŀ�и����ķ�Ӧԭ�����з������
�ڸ���Cװ�õ�Ũ�������CO2���壬����Cװ�û�ʹʵ����ƫ����
�۸��ݱ�����Ϣ��֪����Ӧǰ����ٵ�����Ϊ���ɵĶ�����̼���������������ɵĶ�����̼�������ͻ�ѧ����ʽNa2CO3+H2SO4=Na2SO4+H2O+CO2���������Ʒ��̼���Ƶ�������Ȼ���������������ʽ��ɼ������Ʒ�д��������������
������
��1�����ݳ���Һ������װ�����ܣ�װ���ڵ���ѹ���������ش�
��2����Ӧ���ܲ���ˮ������ʹ����ˮ�����ɳ�ȥ���ɵ������е�ˮ������
��3����ȡ���ʱ����Ͳ������Ҫ����������������ֻ��һ��������
��4���ȸ����������ı���㵪��������������ù�ϵʽ2NaN3��3N2����NaN3��Ʒ�Ĵ��ȣ�
��� �⣺��1��������ײ����30����������NaN3Ѹ�ٷֽ�ΪNa��N2������Ӧ����NaN3����������Na��N2��������ײ�������Է�Ӧ����ʽΪ 2NaN3$\frac{\underline{\;ײ��\;}}{\;}$2Na+3N2����
��2�����������غ㶨�ɣ���Ӧǰ��ԭ�ӵ��������Ŀ���䣬��ȷ������X�Ļ�ѧʽΪ��NH3����������ˮ�γɵİ�ˮ�Լ��ԣ���ʹʪ��ĺ�ɫʯ����ֽ������ʹ��ɫ��̪��Һ���ɫ�����Կ�������ɫ��̪��ֽ���ɫʯ����ֽ��⣻
������̽������
��1����ҵ��NaN3�г�����������Na2CO3����ԭ�����������ƺͿ����еĶ�����̼��Ӧ��Ӧ����̼���ƣ��ʴ�Ϊ��2NaOH+CO2�TNa2CO3+H2O
��2������ƿ�з����ķ�Ӧ����ʽ��Na2CO3+H2SO4=Na2SO4+H2O+CO2����
��Cװ�õ�Ũ�������CO2���壬����Cװ�û�ʹʵ����ƫ��
�۸��ݱ�����Ϣ��֪����Ӧǰ����ٵ�����Ϊ���ɵĶ�����̼��������������̼������=100.00g+241��20g-339.00g=2.2g
����Ʒ��̼���Ƶ�������x��
Na2CO3+H2SO4=Na2SO4+H2O+CO2��
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
̼���Ƶ���������Ϊ��$\frac{5.3g}{100g}$��100%=5.3%
������
��1�����Ӻ�װ�ã���ˮƿעˮ����������Һ�����ұ�Һ���γɸ߶Ȳ���ñ�ǣ�һ��ʱ�����װ�����ܣ�װ������ѹ���䣬���߸߶Ȳ�䣻
��2����Ӧ���ܲ���ˮ������ʹ����ˮ������Ŀ���dz�ȥ���ɵ������е�ˮ������
��3����ȡ���ʱ����Ͳ������Ҫ����������������ֻ��һ������������ѡ100mL����Ͳ��
��4�����ɵ���������Ϊ67.2mL��1000mL/L��1.25g/L=0.084g��
��NaN3��Ʒ�Ĵ���X
2NaN3$\frac{\underline{\;ײ��\;}}{\;}$2Na+3N2����
130 84
X•0.140g 0.084g
$\frac{130}{X��0.140g}=\frac{84}{0.084g}$
��ã�X=92.9%
�𰸣�
��һ����2NaN3$\frac{\underline{\;ײ��\;}}{\;}$2Na+3N2������NH3��
������̽������
��һ����1��2NaOH+CO2�TNa2CO3+H2O�� ��2����Na2CO3+H2SO4=Na2SO4+H2O+CO2������ƫ��5.3%
������
��1���������߳����ȶ���Һ��
��2��ʹˮ����Һ�������ȥˮ��������
��3��A��
��4��92.9%��
���� �ۺ�ʵ���漰֪ʶ��㣬��ѧ��˼ά����Ҫ��ߣ��ȿ���֪ʶ��ʶ�ǡ����⡢Ǩ�ơ����ã��ֿ���������Աȡ����ɵ�˼ά�������������ʽ�������ѧ��������Ҫ��������ĿҪ�ص�ѵ����

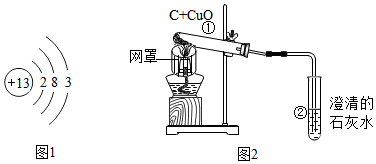
����ʦ���ѡ�����Cu��Fe2O3���ֹ����е�һ�ֻ��������
��������롿��ɫ��ĩ���ܵ���ɣ������ֻ��Cu�� �����ֻ��Fe2O3�� �������Cu��Fe2O3�Ļ����
��ʵ��̽����ͬѧ��Ϊȷ����ɫ��ĩ����ɣ���ȡ�÷�ĩ5.0gװ��Ӳ�ʲ������У���ͼ1��ͨ����н���ʵ�飮��ʼʱ����ͨ��CO���壬��һ��ʱ����ټ���ʹ���ַ�Ӧ������Ӧ��ȫ��ֹͣ���ȣ�����ͨCO����ֱ����������ȴ��
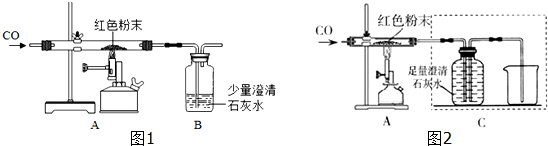
��1����װ��A����ͨCO�����Ŀ�����ž�װ���еĿ�������ֹ����ʱ������ը��Aװ���з�����Ӧ�Ļ�ѧ����ʽΪ3CO+Fe2O3$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2��
��2����Ӧǰ��������װ�ú����ʵ��������������������
| ��Ӧǰ | ��Ӧ�� |
| �����ܺͺ�ɫ��ĩ��������Ϊ37.3g | �����ܺ������ʵ�������Ϊ36.1g |
��3��С��ͬѧ��ΪΪ�˷�ֹ��Һ��������ʵ��ֹͣ����ǰӦ�ȶϿ�A��B�����ӣ�С����Ϊ����Ҫ����������Ϊһֱͨ��CO���壬B����Һ���ᵹ����Aװ���У�
����˼���ۡ�ʵ���С������ͬѧָ������ͼװ��δ����β���Ĵ�����������ͬѧ�������ͼ2װ�ô���ԭװ�ã�ʵ��װ��ͼ�в������߿��ڵ�װ�ã���������AB��
A���ռ�һ����̼ B�����ն�����̼ C�����������̼��
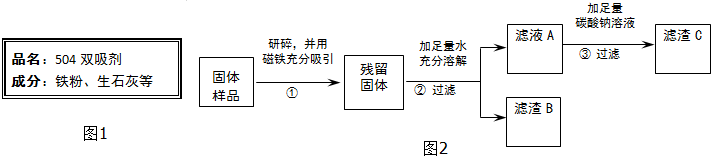
��������⡿���ù���ijɷ���ʲô��
���������ϡ������Ȼ�����Һ�ڳ����·�����Ӧ�����Ȼ�������
���������롿���ù����п��ܺ���Fe��Fe2O3��CaO��Ca��OH��2��CaCO3��
��ʵ��̽����
����ͬѧ�ķ�����
| ʵ����� | ʵ������ | ʵ����� |
| ȡ������������Թ��У��μ�������ϡ���ᣮ | ��������ʧ������ɫ����������õ�dz��ɫ��Һ�� | ������һ������Fe�� һ������Fe2O3�� |
��1���������Ʒ�ô�������ǰ�辭�����飬���������Ŀ��������Ӵ������ʹ��Ӧ��֣�
��2��������й����ܽ�ʱ�ų������ȣ��ɴ˿����жϹ�����һ������CaO��
��3��������з�Ӧ�Ļ�ѧ����ʽ��Na2CO3+Ca��OH��2=CaCO3��+2NaOH��
����ͬѧ������B�ֽ���̽����
| ʵ����� | ʵ������ | ʵ����� |
| ��ȡ����B���Թ��У���������ϡ���� �����ɵ�����ͨ�����ʯ��ˮ | �ٹ�����٣�������ð������Һ��Ϊ��ɫ �ڸ���Һ����ǣ� | ������һ������CaCO3 ��Fe2O3�� |
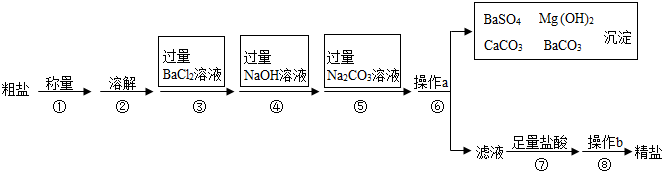
��ʵ����չ��Ϊ��ǿ˫����������Ч��������˫�����м���һ������NaCl��NaCl�����ÿ����Ǽӿ�˫��������������O2�����ʣ�
| A�� | ��˿��������ȼ�գ��������䣬����һ�ֺ�ɫ���� | |
| B�� | ľ̿�ڿ�����ȼ�գ�����һ�ֺ�ɫ���� | |
| C�� | �����ڿ�����ȼ�գ�������ɫ���棬���ɴ����İ�ɫ���� | |
| D�� | �����������ȼ�գ���������ɫ���棬����һ�ִ̼�����ζ������ |
 ������;�㷺����ṹ�����ʵ��ǻ�ѧ����Ҫ�о�����
������;�㷺����ṹ�����ʵ��ǻ�ѧ����Ҫ�о�����