题目内容
硝酸铵受撞击或受热后会发生爆炸性分解,可用作炸药.又因其含氮量比较高,也用做化学肥料.测得某硝酸铵化肥样品中氮元素的质量分数是31.5%,则该化肥样品中硝酸铵的纯度为多少?(杂质中不含有氮元素)
考点:元素的质量分数计算
专题:化学式的计算
分析:先计算出纯净硝酸铵中氮元素的质量分数,再计算样品中NH4NO3的质量分数(即纯度),
依据纯度=
×100%进行解答.
依据纯度=
| 含杂质物质元素的质量分数 |
| 物质中某元素的质量分数 |
解答:解:纯净硝酸铵中氮元素的质量分数=
×100%=35%;
样品中NH4NO3的质量分数为:
×100%=90%;
答:该化肥样品中硝酸铵的纯度为90%.
| 28 |
| 80 |
样品中NH4NO3的质量分数为:
| 31.5% |
| 35% |
答:该化肥样品中硝酸铵的纯度为90%.
点评:将质量分数的计算与生活实际相联系;计算时要理清各个量之间的关系,再结合题意进行分析解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质在空气或氧气中燃烧时,现象描述正确的是( )
| A、在燃着的蜡烛火焰上方,放置一玻璃片,有黑色固体生成 |
| B、铁丝在氧气中燃烧,火星四射,生成四氧化三铁 |
| C、木炭在氧气中燃烧,发出白光,集气瓶内壁出现水雾 |
| D、硫在空气中燃烧,发出明亮的蓝紫色火焰,产生有刺激性气味的气体 |
 如图所示:已知A和E为金属单质,B是化合物且常温下为液态,C具有磁性,F为两性化合物.按要求回答下列问题:
如图所示:已知A和E为金属单质,B是化合物且常温下为液态,C具有磁性,F为两性化合物.按要求回答下列问题: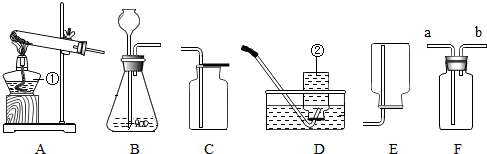
 人体缺乏维生素C(简写“Vc”)就会患坏血病.如图所示为某种“维生素C”说明书的一部分.请回答:
人体缺乏维生素C(简写“Vc”)就会患坏血病.如图所示为某种“维生素C”说明书的一部分.请回答: 玲玲同学在实验室看到一瓶剩余的浓硫酸,标签如左图,为了判断该瓶浓硫酸的溶质质量分数是否改变,她从瓶中取出10毫升浓硫酸,按如图所示进行实验,把10毫升浓硫酸倒入水中变成100克浓硫酸,再加入16克锌粒在烧杯中充分反应后,烧杯内有固体剩余,烧杯内总质量为115.7克.
玲玲同学在实验室看到一瓶剩余的浓硫酸,标签如左图,为了判断该瓶浓硫酸的溶质质量分数是否改变,她从瓶中取出10毫升浓硫酸,按如图所示进行实验,把10毫升浓硫酸倒入水中变成100克浓硫酸,再加入16克锌粒在烧杯中充分反应后,烧杯内有固体剩余,烧杯内总质量为115.7克. A、B、C、D、E、F都是初中化学常见物质,它们之间的关系如图所示(途中“→“表示物质间存在相互转化关系).B是最轻的气体,C是生命源泉,常温下为液态,F有毒,能与血红蛋白结合.
A、B、C、D、E、F都是初中化学常见物质,它们之间的关系如图所示(途中“→“表示物质间存在相互转化关系).B是最轻的气体,C是生命源泉,常温下为液态,F有毒,能与血红蛋白结合.