题目内容
17.市场上一些橡皮、涂改液经检测机构检验后发现甲苯(C7H8)超标34倍.甲苯不但会刺激眼睛、呼吸道,如果在密闭空间里大量吸入,还会造成急性中毒,甚至会致癌.下列有关甲苯的说法错误的是( )| A. | 甲苯中碳、氢元素的质量比为21:2 | |
| B. | 甲苯完全燃烧生成水和二氧化碳 | |
| C. | 甲苯中碳元素的质量分数约为92% | |
| D. | 1个甲苯分子由7个碳原子和8个氢原子构成 |
分析 A.根据化合物中元素质量比的计算方法来分析;
B.根据质量守恒定律来分析;
C.根据化合物中元素质量分数的计算方法来分析;
D.根据化学式的意义来分析.
解答 解:A.甲苯中碳元素和氢元素的质量比是(12×7):(1×8)=21:2,故正确;
B.甲苯由碳元素、氢元素组成的,根据质量守恒定律可知,甲苯完全燃烧生成二氧化碳和水,故正确;
C.甲苯中,碳元素的质量分数为:$\frac{12×7}{12×7+1×8}$×100%≈91.3%,故错误;
D.由甲苯的化学式可知,一个甲苯分子由7个碳原子和8个氢原子构成的,所以说法正确.
故选C.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的意义进行分析问题、解决问题的能力.

练习册系列答案
相关题目
7.下列有关金属的说法错误的是( )
| A. | 金属具有金属光泽,常温下金属都是固体 | |
| B. | 18K金代替纯金来镶嵌宝石,是因为硬度更大 | |
| C. | 炒完菜后,应及时除掉锅底的水,这样可以防止铁锅生锈 | |
| D. | 金属的回收利用是保护金属资源的有效途径之一 |
5.某兴趣小组同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:NaOH溶液滴入酚酞溶液,溶液变成了红色,可是过了一会儿红色就消失了.这是什么原因呢?他们依据所学的化学知识,分别对这种以外现象的成因作了如下猜想:
猜想甲:可能是NaOH溶液与空气中的CO2反应的缘故;
猜想乙:可能是酚酞与空气中的O2反应,使红色消失
猜想丙:可能与NaOH溶液浓度大小有关
(1)老师指出:猜想甲不正确,理由是:CO2与NaOH反应后生成的Na2CO3的溶液也是碱性的,也能使酚酞试液变红色.
(2)为验证猜想乙,同学们进行了如下实验,请填写完整下表:
操作1目的是:赶走溶解在溶液中的O2;
操作2的目的是:防止空气中的O2进入溶液.
(3)若猜想丙正确,请完成下列实验探究:
猜想甲:可能是NaOH溶液与空气中的CO2反应的缘故;
猜想乙:可能是酚酞与空气中的O2反应,使红色消失
猜想丙:可能与NaOH溶液浓度大小有关
(1)老师指出:猜想甲不正确,理由是:CO2与NaOH反应后生成的Na2CO3的溶液也是碱性的,也能使酚酞试液变红色.
(2)为验证猜想乙,同学们进行了如下实验,请填写完整下表:
| 实验操作 | 实验现象 | 实验结论 |
| 1配制较浓的NaOH溶液,并充分加热 | 溶液先变红色,过了一会儿红色仍然消失 | 乙猜想乙错误 (填“正确”或“错误”) |
| 2在加热后的溶液中滴入酚酞,并迅速在上方滴一些植物油 |
操作2的目的是:防止空气中的O2进入溶液.
(3)若猜想丙正确,请完成下列实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 红色消失与NaOH溶液浓度太大有关 |
9.某氮的氧化物中,氮与氧两元素的质量之比为7:20,该氧化物的化学式是( )
| A. | NO | B. | N2O3 | C. | NO2 | D. | N2O5 |
6.充分搅拌后,尚有部分晶体未溶解,稍加热,晶体全部溶解.下列说法正确的是( )
| A. | 搅拌后加热前一定是不饱和溶液 | B. | 搅拌后加热前一定是饱和溶液 | ||
| C. | 加热后一定是不饱和溶液 | D. | 加热后一定是饱和溶液 |
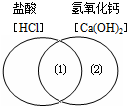 如图是一种用于显示事物异同点的信息处理方法,其中两圆的重叠区域表示物质的相似点,重叠区域以外的部分表示物质的不同点,请写出图中处的适当内容(只要合理即可,每处只要求写一个相似点或不同点).
如图是一种用于显示事物异同点的信息处理方法,其中两圆的重叠区域表示物质的相似点,重叠区域以外的部分表示物质的不同点,请写出图中处的适当内容(只要合理即可,每处只要求写一个相似点或不同点).