题目内容
9.在由A,B两种元素组成的某化合物中,A,与B的质量比为21:8,又知A与B的相对原子质量为7:2,则A,B元素组成的化合物的化学式为( )| A. | A4B3 | B. | A3B2 | C. | A3B4 | D. | A2B3 |
分析 根据题意,元素A和元素B的相对原子质量之比为7:2,在A、B组成的化合物中两元素的质量比为21:8,据此结合化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:元素A和元素B的相对原子质量之比为7:2,在A、B组成的化合物中两元素的质量比为21:8,则A、B组成的化合物的分子中A、B原子的个数比为$\frac{21}{7}$:$\frac{8}{2}$=3:4;该化合物的化学式为:A3B4或B4A3.
故答案为:C.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.根据下面的粒子结构示意图回答问题
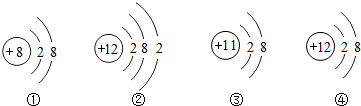
(1)属于原子的是②;
(2)属于阳离子的是③④;
(3)属于阴离子的是①;
(4)属于同种元素的是③④;
(5)具有相似化学性质的是③④;
(6)达到稳定结构的是①③④.

(1)属于原子的是②;
(2)属于阳离子的是③④;
(3)属于阴离子的是①;
(4)属于同种元素的是③④;
(5)具有相似化学性质的是③④;
(6)达到稳定结构的是①③④.
17.归纳与总结是学好化学的重要方法.下列认识中,不完全正确的是( )
| A. | 化学符号与其表示意义 ①Ba2+中的“2”表示一个钡离子带两个单位正电荷 ②2NH3中的“2”表示两个铵根离子 | |
| B. | 物质的性质决定物质的用途 ①磷燃烧能产生白烟--可用于制作烟幕弹 ②氮气化学性质不活泼--可用于食品包装袋内防腐 | |
| C. | 化学知识中有许多“相等” ①化合物中元素化合价的正价总数的数值与负价总数的数值相等 ②参加化学反应的各物质的质量总和与反应后生成的各物质的质量总和相等 | |
| D. | 为更好的利用物质,可对物质进行分离或混合 ①向煤炭中加入石灰石制成型煤,减少空气污染 ②利用蒸馏等方法从海水中提取淡水 |
14.下列叙述不正确的是( )
| A. | 缓慢氧化和燃烧都是氧化反应 | B. | 爆炸都是化学变化 | ||
| C. | 铁丝不能在空气中燃烧 | D. | 油锅着时应立即盖上锅盖 |
18.下列属于纯净物的是( )
| A. | 冰水混合物 | B. | 生铁 | C. | 石灰水 | D. | 空气 |
 过氧化钙晶体较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒.以贝壳为原料制备过氧化钙晶体流程如下:
过氧化钙晶体较稳定,呈白色,微溶于水,广泛应用于环境杀菌、消毒.以贝壳为原料制备过氧化钙晶体流程如下: 如图所示是某同学用高锰酸钾制取氧气的实验装置图,指出装置图中的4处明显错误
如图所示是某同学用高锰酸钾制取氧气的实验装置图,指出装置图中的4处明显错误