题目内容
2.N(NO2)3是科学家2011年发现的一种新型火箭燃料,计算:(1)N(NO2)3中氮原子和氧原子的个数比为2:3;
(2)N(NO2)3的相对分子质量152;
(3)下列化合物中氮元素质量分数最小的是C.
A、N(NO2)3 B、N2O3 C、N2O5
(4)100克N(NO2)3中氮元素的质量与多少克硝酸铵(NH4NO3)中氮元素的质量相等?(结果保留一位小数)
分析 (1)根据1个N(NO2)3分子的构成进行分析解答;
(2)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(3)把每个化学式都变形成只含2个氮原子,与氮原子结合的氧原子的个数越多,氮原子的质量分数越小进行解答;
(4)根据化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:(1)1个N(NO2)3分子中含有4个氮原子和6个氧原子,则N(NO2)3中氮、氧原子个数比是4:6=2:3.故填:2:3;
(2)N(NO2)3的相相对分子质量=14×4+16×6=152;故填:152;
(3)根据各化学式:A.N(NO2)3--N2O3 ,B.N2O3,C.N2O5,则可知:每2个氮原子结合氧原子最多的是N2O5;
故选C;
(4)设硝酸铵的质量为x,则
100g×$\frac{14×4}{152}×100%$=x×$\frac{14×2}{80}×100%$
x=105.3g
答:硝酸铵的质量为105.3g.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
13.2015年10月,中国科研团队首次证实了天然铀单质的存在.用于核电工业的一种铀原子中含有92个质子和143个中子.有关该原子的说法不正确的是( )
| A. | 属于金属元素 | B. | 原子序数为92 | ||
| C. | 核外电子数为92 | D. | 相对原子质量为143 |
17.2017年5月18日国土资源地质调查局宣布:正在南海北部神狐海域进行的可燃冰试采获得成功.可燃冰又称天然气水合物,其晶体中平均每46个水分子构建成8个笼,每个笼内可容纳1个甲烷分子或1个游离的水分子.若晶体中每8个笼有6个容纳了甲烷分子,另外两个被水分子填充,则“可燃冰”的化学式可表示为( )
| A. | CH4•5H2O | B. | CH4•6H2O | C. | CH4•7H2O | D. | CH4•8H2O |
14.某研究性学习小组的甲、乙两名同学分别从室温的一瓶硝酸钾不饱和溶液中各取出100g和80g,他们将各自所取的溶液恒温蒸发掉20g水后,经测定乙同学所剩余溶液刚好成为室温时的饱和溶液.请分析,此时甲同学所剩余溶液是( )
| A. | 室温的饱和溶液 | |
| B. | 室温时的不饱和溶液 | |
| C. | 室温时的不饱和溶液,且有晶体析出 | |
| D. | 室温时的饱和溶液,且有晶体析出 |
11.根据所给的化学反应,填写化学方程式,并回答有关问题:
| 化学反应 | 化学方程式 | 简答 |
| 二氧化碳通 入灼热的碳 | C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO | 反应类型化合反应 |
| 硫在空气中 燃烧 | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 | 观察到的现象剧烈燃烧,发出微弱的淡蓝色火焰 |
| 氯酸钾与二 氧化锰共热 | 2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | 加热时试管口应稍微向下倾斜 |
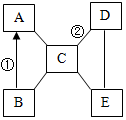 A、B、C、D、E是初中化学常见五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E广泛用于玻璃、造纸、纺织和洗涤剂的生产等,图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去,回答下列问题:
A、B、C、D、E是初中化学常见五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E广泛用于玻璃、造纸、纺织和洗涤剂的生产等,图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去,回答下列问题: