题目内容
某NaCl、Na2CO3的固体混合物22.8g,完全溶于136g水配制成溶液,向该溶液中加入100g稀盐酸恰好完全反应,共收集到气体8.8g,若实验中没有任何物质损失,试计算:
(1)原混合物中NaCl的质量
(2)稀盐酸中溶质的质量分数
(3)最终溶液中溶质的质量分数.
解:(1)设碳酸钠的质量为x,盐酸中溶质的质量为y,生成氯化钠的质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x y z 8.8g
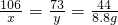
解之得:x=21.2g,y=14.6g,z=23.4g
原混合物中NaCl的质量为:22.8g-21.2g=1.6g;
(2)稀盐酸中溶质的质量分数为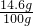 ×100%=14.6%;
×100%=14.6%;
(3)最终溶液中溶质的质量分数为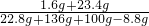 ×100%=10%.
×100%=10%.
答:(1)原混合物中NaCl的质量为1.6g;
(2)稀盐酸中溶质的质量分数14.6%;
(3)最终溶液中溶质的质量分数10%.
分析:(1)根据生成的二氧化碳的质量结合反应的化学方程式可以求算出碳酸钠的质量,进而计算出氯化钠的质量;
(2)根据生成的二氧化碳的质量结合反应的化学方程式可以求算出盐酸中氯化氢的质量,然后计算出稀盐酸的质量分数即可;
(3)根据碳酸钠和盐酸反应的化学方程式可以知道溶液中的溶质为氯化钠,注意氯化钠有两个来源,即反应中生成的和反应前加入的,可以据此进行解答.
点评:本题主要考查学生运用化学方程式进行计算,要分清溶液中的溶质既有原来的样品中的也有反应生成的然后根据碳酸钠和稀盐酸反应的化学方程式计算可得,溶液的质量根据质量守恒定律算出生成的气体用所有加入反应器中的物质的总质量减去气体即是,但要注意反应中生成的气体要减去.
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x y z 8.8g
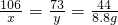
解之得:x=21.2g,y=14.6g,z=23.4g
原混合物中NaCl的质量为:22.8g-21.2g=1.6g;
(2)稀盐酸中溶质的质量分数为
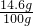 ×100%=14.6%;
×100%=14.6%;(3)最终溶液中溶质的质量分数为
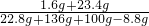 ×100%=10%.
×100%=10%.答:(1)原混合物中NaCl的质量为1.6g;
(2)稀盐酸中溶质的质量分数14.6%;
(3)最终溶液中溶质的质量分数10%.
分析:(1)根据生成的二氧化碳的质量结合反应的化学方程式可以求算出碳酸钠的质量,进而计算出氯化钠的质量;
(2)根据生成的二氧化碳的质量结合反应的化学方程式可以求算出盐酸中氯化氢的质量,然后计算出稀盐酸的质量分数即可;
(3)根据碳酸钠和盐酸反应的化学方程式可以知道溶液中的溶质为氯化钠,注意氯化钠有两个来源,即反应中生成的和反应前加入的,可以据此进行解答.
点评:本题主要考查学生运用化学方程式进行计算,要分清溶液中的溶质既有原来的样品中的也有反应生成的然后根据碳酸钠和稀盐酸反应的化学方程式计算可得,溶液的质量根据质量守恒定律算出生成的气体用所有加入反应器中的物质的总质量减去气体即是,但要注意反应中生成的气体要减去.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
为测定某NaCl、Na2CO3固体混合物的组成,小明同学取16 g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下面的质量关系:
请分析以上数据后计算:
(1)原固体混合物中Na2CO3的质量.
(2)当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数.(计算结果精确到0.1)
| 加入稀盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 烧杯及反应后混合物的总质量/g | 122.2 | 146.1 | 170.0 | 193.9 | 218.9 |
(1)原固体混合物中Na2CO3的质量.
(2)当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数.(计算结果精确到0.1)
为测定某NaCl、Na2CO3固体混合物的组成,小明同学取16 g该混合物放入烧杯中,分五次加入稀盐酸(每次加入稀盐酸的质量为25g),待反应完全后,得到下面的质量关系:
请分析以上数据后计算:
(1)原固体混合物中Na2CO3的质量.
(2)当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数.(计算结果精确到0.1)
| 加入稀盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 | 第五次 |
| 烧杯及反应后混合物的总质量/g | 122.2 | 146.1 | 170.0 | 193.9 | 218.9 |
(1)原固体混合物中Na2CO3的质量.
(2)当加入稀盐酸至固体混合物恰好完全反应时,所得溶液的溶质质量分数.(计算结果精确到0.1)