题目内容
如图甲是硝酸钾的溶解度曲线,在20℃时,向20g水中溶解一定量KNO3固体的操作如图乙所示.下列说法正确的是( )
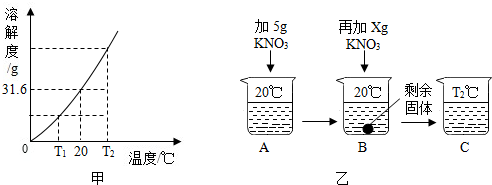

| A、由图甲可知,在20℃时,100g硝酸钾饱和溶液中含有31.6g硝酸钾 |
| B、烧杯A中溶液的溶质质量分数是25% |
| C、若要使B烧杯中恰好没有固体剩余,则X的值为1.32 |
| D、将20℃时的硝酸钾饱和溶液(无固体剩余)升温至T2℃,溶质的质量分数会增大 |
考点:固体溶解度曲线及其作用,溶质的质量分数
专题:溶液、浊液与溶解度
分析:A、由溶解度曲线图可以看出在某温度时物质的溶解度;
B、据溶质的质量分数计算方法解答;
C、据该温度下硝酸钾的溶解度分析解答;
D、据硝酸钾的溶解度随温度变化情况分析解答.
B、据溶质的质量分数计算方法解答;
C、据该温度下硝酸钾的溶解度分析解答;
D、据硝酸钾的溶解度随温度变化情况分析解答.
解答:解:A、20℃时,KNO3的溶解度是31.6g,即131.6g饱和溶液中最多溶解31.6g的硝酸钾,故错误;
B、20℃时,KNO3的溶解度是31.6g,则20g水中最多溶解溶质的质量是20g×
=6.32g,所以A溶液中加入5g硝酸钾可全部溶解,溶质的质量分数是:
×100%=20%,故错误;
C、温度不变,若要使B烧杯中恰好没有固体剩余,则X的值为6.32g-5g=1.32g,正确;
D、从图中可以看出硝酸钾的溶解度随温度升高而增大,所以20℃时,KNO3的饱和溶液(无固体剩余)升温至T2℃,溶质的质量分数不变,故错误;
故选:C.
B、20℃时,KNO3的溶解度是31.6g,则20g水中最多溶解溶质的质量是20g×
| 31.6g |
| 100g |
| 5g |
| 15g |
C、温度不变,若要使B烧杯中恰好没有固体剩余,则X的值为6.32g-5g=1.32g,正确;
D、从图中可以看出硝酸钾的溶解度随温度升高而增大,所以20℃时,KNO3的饱和溶液(无固体剩余)升温至T2℃,溶质的质量分数不变,故错误;
故选:C.
点评:本题考查了学生运用溶解度概念、溶解度曲线的相关知识分析、解决问题的能力.

练习册系列答案
相关题目
如图为某反应的微观示意图,下列说法不正确的是( )


| A、反应后的物质是混合物 | ||||
| B、该反应中AB与B2的分子个数比为2:3 | ||||
| C、该反应属于化合反应 | ||||
D、该反应可以表示为2AB+B2
|
将含有少量泥沙的粗盐提纯,并用制得的精盐配制一定质量分数的氯化钠溶液.下列说法错误的是( )
| A、过滤时搅拌漏斗中的液体可以加快过滤速度 |
| B、蒸发滤液时,要不断用玻璃棒搅动蒸发皿中的液体 |
| C、配制氯化钠溶液的实验过程需要经过计算、称量、溶解、等步骤 |
| D、在量取一定体积水时,如仰视刻度,则配制的食盐溶液的溶质质量分数会偏小 |
 某学习小组用右图做镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.
某学习小组用右图做镁条在空气中燃烧的实验,燃烧、冷却后打开止水夹,进入集气瓶中水的体积约占集气瓶体积的70%.