题目内容
13.造纸是我国古代四大发明之一,它有效地推动了人类文明的发展.(1)回收农田产生的秸秆作为造纸原料,可以减少焚烧秸秆带来的大气污染.秸秆的主要成分是纤维素[(C6H10O5)n],纤维素中各元素的质量比为36:5:40(用最简整数比表示).
(2)造纸会产生大量含NaOH的碱性废水,需经处理呈中性后再排放.若某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸19.6t(H2SO4的质量分数为20%),可以处理的废水质量是多少?
分析 (1)焚烧秸秆会带来大气污染,化学式中各元素的质量比为各元素的相对原子质量×原子个数的之比,据此分析计算回答.
(2)可先根据化学方程式求出氢氧化钠的质量,在根据废水中氢氧化钠的质量分数求出废水的质量.
解答 解:
(1)焚烧秸秆会产生大量烟尘等,污染空气;根据纤维素的化学式(C6H1005)n知,纤维素中C、H、O三种元素的质量比=(12×6):(1×10):(16×5)=36:5:40.
(2)19.6t废硫酸溶液中含硫酸的质量为19.6t×20%=3.92t
设19.6t废硫酸溶液可以反应氢氧化钠的质量为x
H2SO4 +2NaOH=Na2SO4 +2H2O
98 80
3.92t x
$\frac{98}{3.92t}=\frac{80}{x}$
解之得:x=3.2t
含1.6t氢氧化钠的废水的质量=$\frac{3.2t}{1.6%}$=200t
故答案为:
(1)大气,36:5:40;(2)可以处理的废水质量是200t.
点评 本题主要考查化学式的含义及根据化学方程式进行简单计算的能力.难度不大,根据已有的知识即可分析解答.

练习册系列答案
相关题目
3. 科学家发现,氧气可以通过高能真空紫外线照射二氧化碳直接产生,该化学反应的微观模型如图所示,关于该反应的说法错误的是 ( )
科学家发现,氧气可以通过高能真空紫外线照射二氧化碳直接产生,该化学反应的微观模型如图所示,关于该反应的说法错误的是 ( )
 科学家发现,氧气可以通过高能真空紫外线照射二氧化碳直接产生,该化学反应的微观模型如图所示,关于该反应的说法错误的是 ( )
科学家发现,氧气可以通过高能真空紫外线照射二氧化碳直接产生,该化学反应的微观模型如图所示,关于该反应的说法错误的是 ( )| A. | 属于分解反应 | B. | 反应中的最小粒子是分子 | ||
| C. | 该反应符合质量守恒定律 | D. | 为制取氧气提供了新的方法 |
1.如图是氯化铵和氢氧化钠在不同温度下的溶解度:
(1)氯化铵和氢氧化钠的溶解度曲线不能(填“能”或“不能”)相交.
(2)70℃时,等质量的饱和氯化铵、氢氧化钠溶液分别降温至20℃,析出晶体NaOH多,所得溶液中的溶剂是NH4Cl溶液多.
(3)将70℃时的饱和氯化铵、氢氧化钠溶液充分混合,观察到有刺激性氨味,有气体冒出,有晶体析出.
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度 | NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.0 | 60.2 |
| NaOH | 42 | 51 | 109 | 119 | 129 | 145 | 174 | 299 | |
(2)70℃时,等质量的饱和氯化铵、氢氧化钠溶液分别降温至20℃,析出晶体NaOH多,所得溶液中的溶剂是NH4Cl溶液多.
(3)将70℃时的饱和氯化铵、氢氧化钠溶液充分混合,观察到有刺激性氨味,有气体冒出,有晶体析出.
18.小洁整理的下列知识中,归类正确的是( )
| A. | 可燃性气体:天然气、一氧化碳、氧气 | |
| B. | 常用的溶剂:水、酒精、汽油 | |
| C. | 合成材料:塑料、棉花、合成橡胶 | |
| D. | 还原剂:氢气、碳、二氧化碳 |
5.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式2NaOH+H2SO4═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想 针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想四,氢氧化钠和硫酸不能同时剩余.
【继续实验】
(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是测pH时将pH试纸伸进了溶液内;
(2)实验方案探究中也有一个是不合理的,不合理的原因是硫酸钠能与氯化钡反应产生白色沉淀.
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式2NaOH+H2SO4═Na2SO4+2H2O.
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想 针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想四,氢氧化钠和硫酸不能同时剩余.
【继续实验】
(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 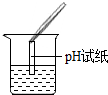 | 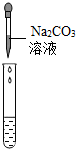 | 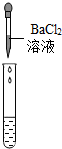 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是测pH时将pH试纸伸进了溶液内;
(2)实验方案探究中也有一个是不合理的,不合理的原因是硫酸钠能与氯化钡反应产生白色沉淀.
3.“珍爱生命,远离毒品”.冰毒是一种毒品,其主要成分是甲基苯丙胺(化学式为C10H15N).有关甲基苯丙胺的说法错误的是( )
| A. | 属于纯净物 | |
| B. | 燃烧后只生成二氧化碳和水 | |
| C. | 甲基苯丙胺由碳、氢、氮元素组成 | |
| D. | 1个甲基苯丙胺分子由10个碳原子、15个氢原子和1个氮原子组成 |

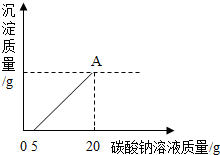 为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示:
为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液20克于烧杯中,在不断振荡的条件下,向其中滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示: