题目内容
某碳的氧化物中,碳元素和氧元素的质量比为3:4,对这种氧化物中各元素的关系叙述正确的是A.碳元素与氧元素的原子个数比为1:1 B.碳元素的质量分数为27.27%
C.28g该氧化物中含碳元素的质量为14g D. .
【答案】分析:根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,化合物中元素的质量分数= ×100%,化合物中某元素的质量=化合物的质量×该元素的质量分数,进行解答.
×100%,化合物中某元素的质量=化合物的质量×该元素的质量分数,进行解答.
解答:解:A、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;可得C,O原子个数之比为: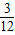 :
: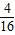 =1:1,由此可知,氧化物的化学式为CO;故叙述正确;
=1:1,由此可知,氧化物的化学式为CO;故叙述正确;
B、氧化物中碳元素的质量分数= ×100%=42.9%,故叙述错误;
×100%=42.9%,故叙述错误;
C、28g该氧化物中含碳元素的质量为28g×42.9%=12g,故叙述错误;
D、氧化物中氧元素的质量分数=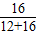 ×100%=57.1%;
×100%=57.1%;
故选:A;补充:氧元素的质量分数为57.1%.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.
 ×100%,化合物中某元素的质量=化合物的质量×该元素的质量分数,进行解答.
×100%,化合物中某元素的质量=化合物的质量×该元素的质量分数,进行解答.解答:解:A、根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比;可得C,O原子个数之比为:
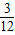 :
: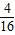 =1:1,由此可知,氧化物的化学式为CO;故叙述正确;
=1:1,由此可知,氧化物的化学式为CO;故叙述正确;B、氧化物中碳元素的质量分数=
 ×100%=42.9%,故叙述错误;
×100%=42.9%,故叙述错误;C、28g该氧化物中含碳元素的质量为28g×42.9%=12g,故叙述错误;
D、氧化物中氧元素的质量分数=
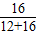 ×100%=57.1%;
×100%=57.1%;故选:A;补充:氧元素的质量分数为57.1%.
点评:本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目