题目内容
下图是a、b、c三种物质的溶解度曲线,下列分析正确的是
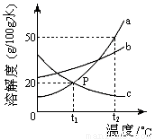
A.t1 ℃时,100g a物质饱和溶液中含有20g a物质
B.t2 ℃时a、c两种物质的饱和溶液中溶质相等
C.将t2 ℃时a、b、c三种物质的饱和溶液降温至t1 ℃时,所得溶液的溶质质量分数关系是b>a〉c
D.a物质中含有少量的b物质,可采用冷却热饱和溶液的方法
CD
【解析】
试题分析:A、t1 ℃时,120g a物质饱和溶液中含有20g a物质,错误;B、t2 ℃时a物质溶解度大于c物质溶解度,则两物质饱和溶液中溶质不相等,错误;C、将t2 ℃时a、b、c三种物质溶解度的大小关系为:a > b 〉 c;降温至t1 ℃时c为不饱和溶液,a、b为饱和溶液,c为不饱和溶液,其溶质质量分数和t2 ℃时一样,a、b量物质溶解度大小关系为:b> a,此时三种溶液溶质质量分数b >a 〉 c,正确;D、a溶解度受温度影响变化较大,采用冷却热饱和溶液的方法提纯a,正确。故选CD
考点:溶解度曲线应用,溶质质量分数,结晶方法。

下表是常见的几种酸、碱、盐在水溶液中解离出来离子的情况,根据表中信息分析,得出的结论正确的是
溶液 | 酸 | 盐 | 碱 | ||||
HCl | H2SO4 | NaCl | NaHSO4 | NH4Cl | NaOH | NH3H2O | |
解离出来的 离子 | H+,Cl﹣ | H+,SO42- | Na+,Cl﹣ | Na+,H+, SO42- | NH4+,Cl﹣ | Na+,OH﹣ | NH4+,OH﹣ |
A.在水溶液中能解离出H+的物质一定是酸
B.在水溶液中解离出金属阳离子和酸根离子的物质一定是盐
C.碱溶液中一定存在金属阳离子和OH﹣
D.盐溶液中一定存在金属阳离子和酸根离子
比较、推理是化学学习常用的方法,以下是根据一些反应事实推导出的影响化学反应的因 素,其中推理不合理的是
素,其中推理不合理的是
序号 | 化学反应事实 | 影响化学反应的因素 |
A | 铁丝在空气中很难燃烧,而在氧气中能剧烈燃烧 | 氧气的浓度 |
B | 碳在常温下不与氧气发生反应,而在点燃时能与氧气反应 | 反应温度 |
C | 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |