题目内容
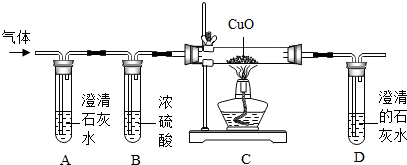
11.在学生创新实验大赛中,某同学设计了如图气体制取与性质验证的综合实验,打开A中分液漏斗的活塞,很快看到E中导管口有气泡冒出,且溶液由紫色变红色,请看图回答问题: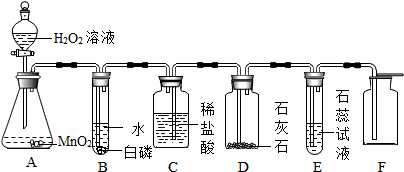
(1)A中反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)B中白磷不燃烧,原因是温度没有达到着火点.
(3)用化学方程式表示E中颜色变化的原因CO2+H2O=H2CO3;
(4)用F装置收集气体的依据是密度比空气大;
(5)若保证以上实验顺利进行,实验前必须检查装置的气密性.
分析 (1)根据实验装置来确定制取气体的方法;
(2)根据可燃物燃烧的条件来分析;
(3)根据二氧化碳的性质来分析;
(4)根据气体收集方法选择依据来分析;
(5)根据实验室制取气体的步骤进行分析解答.
解答 解:(1)该装置适用于固体与液体在常温的条件下反应来制取氧气,故为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)B中的白磷虽然与氧气接触,但是其温度没有达到着火点,所以没有发生燃烧;故填:温度没有达到着火点;
(3)二氧化碳与水反应生成碳酸,碳酸能使紫色的石蕊试液变红色;故填:CO2+H2O=H2CO3;
(4)二氧化碳的密度比空气大,所以可以用向上排空气法来收集二氧化碳;故填:密度比空气大;
(5)实验室制取气体时,组装好装置后,应在向容器中装入药品前检查装置的气密性,然后再装入药品.避免装入药品后发现装置气密性不好,更换部分仪器而浪费药品.故答案是:检查装置的气密性.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
19.K2CO3是草木灰的主要成分,下列说法正确的是( )
| A. | K2CO3中钾、碳、氧三种元素的质量之比为2:1:3 | |
| B. | K2CO3中碳元素的质量分数为$\frac{12}{39+12+16}$×100% | |
| C. | K2CO3的相对分子质量为138 | |
| D. | K2CO3溶液能导电,是因为溶液中存在大量自由移动的分子 |
3.分析推理是学习化学常用的一种方法,下列推理不正确的是( )
| A. | 碱的溶液呈碱性,呈碱性的溶液一定是碱的溶液 | |
| B. | 氧化物中含有氧元素,但含氧元素的化合物不一定是氧化物 | |
| C. | 离子是带电粒子,但带电的粒子不一定是离子 | |
| D. | 中和反应一定是复分解反应 |
20.回答下列实验中的有关问题.
(1)A中玻璃棒的作用是散发热量.
(2)B中较长一段时间后,可观察到的现象是铁丝表面附着红色固体,试管内页面上升.
(3)C中可观察到的现象是红磷燃烧,产生白烟,打开弹簧夹,烧杯中部分水进入瓶中,进入水的体积约占集气瓶容积的五分之一,反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
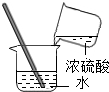 | 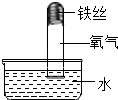 | 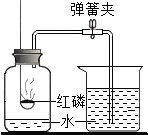 |
| A | B | C |
(2)B中较长一段时间后,可观察到的现象是铁丝表面附着红色固体,试管内页面上升.
(3)C中可观察到的现象是红磷燃烧,产生白烟,打开弹簧夹,烧杯中部分水进入瓶中,进入水的体积约占集气瓶容积的五分之一,反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
16.下列实验现象的预测或分析中,错误的是( )
| A. | 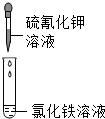 试管中溶液颜色变成红色 | |
| B. | 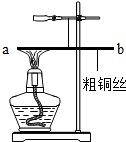 系于细线下原来保持水平的粗铜丝,经过加热、冷却后b端略上升 | |
| C. | 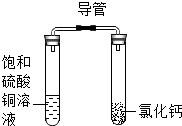 放置一段时间后,饱和硫酸铜溶液中出现蓝色晶体 | |
| D. | 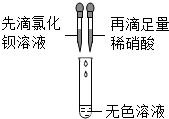 若出现白色沉淀且沉淀不消失,说明无色溶液中一定含硫酸根离子 |
 今年3月,山东济南非法经营疫苗案引起全社会的广泛关注.
今年3月,山东济南非法经营疫苗案引起全社会的广泛关注.
