题目内容
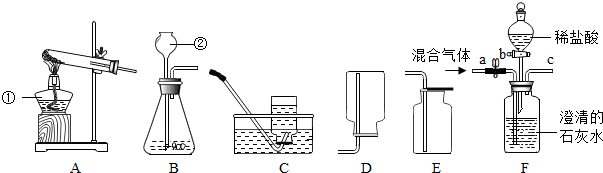
下列是初中化学常见的基本实验.请回答以下问题:

(1)实验一可用于测定空气中氧气的含量.下列说法不正确的是 (填序号);
A.实验时红磷要过量 B.可用木炭代替红磷完成实验
C.火焰熄灭后要立刻打开弹簧夹,观察水面变化情况
D.该实验可以证明氧气约占空气总体积的
E.通过该实验还可以了解氮气的一些性质
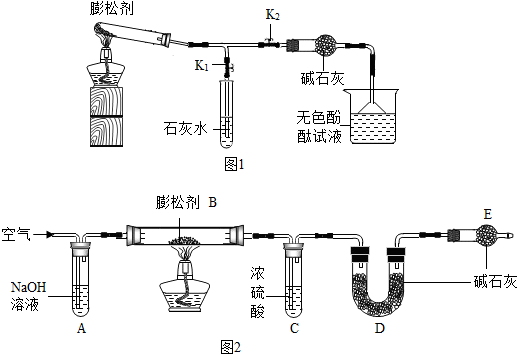
(2)实验二中,两液体混合后所发生反应的化学方程式为 .该实验 (填“能”或“不能”)验证质量守恒定律
(3)实验三中,玻璃管内的现象是 ;
(4)实验四完成氢气还原氧化铜的实验时,要先 (填序号);
A.通一会儿氢气 B.点燃酒精灯
该实验中所发生反应的化学方程式为 .

(1)实验一可用于测定空气中氧气的含量.下列说法不正确的是
A.实验时红磷要过量 B.可用木炭代替红磷完成实验
C.火焰熄灭后要立刻打开弹簧夹,观察水面变化情况
D.该实验可以证明氧气约占空气总体积的
| 1 |
| 5 |
(2)实验二中,两液体混合后所发生反应的化学方程式为
(3)实验三中,玻璃管内的现象是
(4)实验四完成氢气还原氧化铜的实验时,要先
A.通一会儿氢气 B.点燃酒精灯
该实验中所发生反应的化学方程式为
考点:空气组成的测定,一氧化碳还原氧化铁,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式,氢气的化学性质与燃烧实验
专题:实验性简答题
分析:(1)根据测定空气中氧气含量的实验应该注意的事项分析;
(2)根据反应物和复分解反应的条件来书写方程式;
(3)根据在高温条件一氧化碳与氧化铜的反应分析实验的现象;
(4)氢气还原氧化铜时,反应前,试管口略向下倾斜,将氢气验纯后先通一段时间氢气,然后再加热;在加热的条件下氧化铜与氢气反应生成铜和水.
(2)根据反应物和复分解反应的条件来书写方程式;
(3)根据在高温条件一氧化碳与氧化铜的反应分析实验的现象;
(4)氢气还原氧化铜时,反应前,试管口略向下倾斜,将氢气验纯后先通一段时间氢气,然后再加热;在加热的条件下氧化铜与氢气反应生成铜和水.
解答:解:(1)测定空气中氧气含量时,红磷一定要过量才能保证将装置内的氧气完全耗尽;因为木炭燃烧会生成二氧化碳气体,不能用木炭来代替红磷;当红磷燃烧熄灭冷却至室温后,才能打开止水夹;该实验还验证了氮气难溶于水,不燃烧也不支持燃烧等性质;故填:BC;
(2)氯化钙与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,因为该反应中没有气体参与,也没有气体产生,故可用来验证质量守恒定律;故填:Na2CO3+CaCl2=CaCO3↓+2NaCl;能;
(3)由于在高温条件下,一氧化碳将氧化铁还原成铁,所以,实验的现象是:红色粉末逐渐变成黑色.故填:红色粉末逐渐变成黑色;
(4)实验开始时,先通入氢气,待试管中的空气被排净后,再给氧化铜加热,以防试管内的混合气体受热发生爆炸;在加热的条件下氧化铜与氢气反应生成铜和水.故填:A;CuO+H2
Cu+H2O.
(2)氯化钙与碳酸钠反应生成碳酸钙白色沉淀和氯化钠,因为该反应中没有气体参与,也没有气体产生,故可用来验证质量守恒定律;故填:Na2CO3+CaCl2=CaCO3↓+2NaCl;能;
(3)由于在高温条件下,一氧化碳将氧化铁还原成铁,所以,实验的现象是:红色粉末逐渐变成黑色.故填:红色粉末逐渐变成黑色;
(4)实验开始时,先通入氢气,待试管中的空气被排净后,再给氧化铜加热,以防试管内的混合气体受热发生爆炸;在加热的条件下氧化铜与氢气反应生成铜和水.故填:A;CuO+H2
| ||
点评:根据所给的实验、问题情景,结合所学的相关知识和技能,联系起来细心地探究、推理后,按照题目要求进行选择或解答即可.

练习册系列答案
相关题目
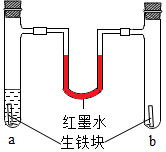 在a、b两支试管中加入体积相同的同种铁块.在a中加入食盐水,塞上橡皮塞,如图.U型玻璃管内为红墨水(开始时两端液面等高).放置一段时间后,下列有关叙述错误的是( )
在a、b两支试管中加入体积相同的同种铁块.在a中加入食盐水,塞上橡皮塞,如图.U型玻璃管内为红墨水(开始时两端液面等高).放置一段时间后,下列有关叙述错误的是( )| A、两试管中铁最终均被锈蚀 |
| B、红墨水柱两边的液面变为左低右高 |
| C、若在a试管水面上加少量植物油,可使其锈蚀变慢 |
| D、铁锈是混合物,主要成分是Fe2O3 |

 汽车是现代生活中不可缺少的代步工具.请回答下列问题?
汽车是现代生活中不可缺少的代步工具.请回答下列问题?