题目内容
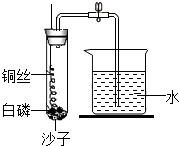 为测定空气中氧气与氮气的体积比,某同学设计了如图所示的装置进行实验.具体操作是:先关闭弹簧夹;再将螺旋状的铜丝在酒精灯上灼烧后迅速插入大试管接触试管底部的白磷(过量);然后立即塞紧橡胶塞.他观察到大试管中产生大量的白烟.请你帮他解答下列问题:
为测定空气中氧气与氮气的体积比,某同学设计了如图所示的装置进行实验.具体操作是:先关闭弹簧夹;再将螺旋状的铜丝在酒精灯上灼烧后迅速插入大试管接触试管底部的白磷(过量);然后立即塞紧橡胶塞.他观察到大试管中产生大量的白烟.请你帮他解答下列问题:(1)写出自磷燃烧的化学方程式
(2)待试管冷却后打开弹簧夹,此时可观察到的现象为
(3)如果装置气密性不好,测出氧气与氮气的体积比将
考点:空气组成的测定,书写化学方程式、文字表达式、电离方程式
专题:空气与水
分析:(1)默写白磷燃烧的化学方程式;
(2)根据白磷燃烧生成白色固体五氧化二磷而使试管内气体体积减小,结合空气中氧气含量分析实验中出现的现象,并利用对压强的认识解释出现该现象的原因;
(3)分析装置气密性不好在冷却过程中可能出现的意外,判断该意外情况对实验测出氧气与氮气的体积比的影响.
(2)根据白磷燃烧生成白色固体五氧化二磷而使试管内气体体积减小,结合空气中氧气含量分析实验中出现的现象,并利用对压强的认识解释出现该现象的原因;
(3)分析装置气密性不好在冷却过程中可能出现的意外,判断该意外情况对实验测出氧气与氮气的体积比的影响.
解答:解:
(1)白磷在空气中燃烧,与空气中氧气反应生成五氧化二磷,反应的化学方程式为4P+5O2
2P2O5;
(2)白磷燃烧消耗氧气,待试管冷却后,由于占空气体积
的氧气被完全反应,管内气体体积减小,使试管内压强减小的缘故,打开弹簧夹,水倒流入试管内,填补原来氧气所占体积,因此进入的水的体积约占试管容积的
;据此可证实空气中O2与N2的体积比大约为 1:4.
(3)如果装置气密性不好,在进行冷却过程中,外界空气进入试管,而导致进入水的体积偏小,则测出氧气与氮气的体积比偏小;
故答案为:
(1)4P+5O2
2P2O5
(2)水倒流入试管内,约占试管容积的
; 1:4
(3)偏小
(1)白磷在空气中燃烧,与空气中氧气反应生成五氧化二磷,反应的化学方程式为4P+5O2
| ||
(2)白磷燃烧消耗氧气,待试管冷却后,由于占空气体积
| 1 |
| 5 |
| 1 |
| 5 |
(3)如果装置气密性不好,在进行冷却过程中,外界空气进入试管,而导致进入水的体积偏小,则测出氧气与氮气的体积比偏小;
故答案为:
(1)4P+5O2
| ||
(2)水倒流入试管内,约占试管容积的
| 1 |
| 5 |
(3)偏小
点评:利用可燃物耗尽空气中氧气,测量所剩余气体的体积而得到空气中氧气的体积分数,实验中要求可燃物燃烧不能产生新的气体.

练习册系列答案
相关题目
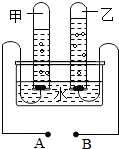 如图是电解水的实验装置图,请根据你所了解的知识填空:
如图是电解水的实验装置图,请根据你所了解的知识填空: