题目内容
1.青岩古镇不但其传统文化吸引各方游客,她的笑食也让不少游客流连忘返.请从化学视角冋答下列问题.(1)闻到青岩卤猪脚浓郁香味,说明分子总是不断运动的.
(2)“鸡辣椒”“米豆腐”“洋芋耙”“玫瑰糖”“豆腐圆子”“丝娃娃”等也很具特色,这些食物中含有的营养素有糖类、蛋白质、维生素(至少写出两种).
(3)米豆腐的制作中要放入适量生石灰,故吃米豆腐时往往要加适量的醋,原因是中和生石灰生成的碱性.
(4)“玫瑰糖”中的糖主要是麦芽糖,其化学式为C12H12O11,由该化学式能获得的信息有由碳、氢、氧三种元素组成的;1个玫瑰糖分子中含有12个碳原子、12个氢原子和11个氧原子,共35个;玫瑰糖的相对分子质量为为12×12+1×12+16×11=332;玫瑰糖中碳、氢、氧元素的质量比=12×12:1×12:16×11=72:11:88.
分析 (1)根据微观粒子的特征进行分析;
(2)人类需要的营养物质有糖类、油脂、蛋白质、维生素、水和无机盐,根据各营养素的食物来源进行分析;
(3)根据生石灰遇水变成氢氧化钙显碱性分析;
(4)根据麦芽糖的化学式的意义进行分析.
解答 解:(1)闻到青岩卤猪脚浓郁香味,说明分子总是不断运动的;
(2)鸡辣椒中富含维生素,米豆腐、豆腐圆子中富含蛋白质,洋芋耙中富含淀粉,淀粉属于糖类,玫瑰糖中富含糖类,丝娃娃中富含糖类、油脂和维生素等;
(3)米豆腐的制作中要放入适量生石灰,故吃米豆腐时往往要加适量的醋以中和生石灰生成的碱性;
(4)玫瑰糖的化学式为C12H12O11,可见它是由碳、氢、氧三种元素组成的;1个玫瑰糖分子中含有12个碳原子、12个氢原子和11个氧原子,共35个;玫瑰糖的相对分子质量为为12×12+1×12+16×11=332;玫瑰糖中碳、氢、氧元素的质量比=12×12:1×12:16×11=72:11:88.
故答案为:(1)总是不断运动的;(2)糖类、蛋白质、维生素;(3)中和生石灰生成的碱性;(4)由碳、氢、氧三种元素组成的;1个玫瑰糖分子中含有12个碳原子、12个氢原子和11个氧原子,共35个;玫瑰糖的相对分子质量为为12×12+1×12+16×11=332;玫瑰糖中碳、氢、氧元素的质量比=12×12:1×12:16×11=72:11:88.
点评 本题考查微粒的特性,物质含有的营养元素,化学式表示的意义等,难度不大.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目
12.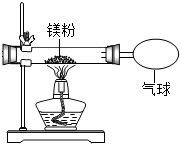 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量火于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为镁燃烧是镁与空气中氧气等的反应.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
【反思与交流】空气中N2的含量远大于02的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2.请给出合理的解释氧气的化学性质比氮气更活泼,镁条更容易与氧气发生反应,写出生成Mg3N2的化学方程式3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.(1)请写出镁条与氧气反应的化学方程式2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
(2)小明发现燃烧产物的质量火于反应物镁条的质量,认为这个反应不遵循质量守恒定律.我不同意(“同意”或“不同意”)小明的观点,因为镁燃烧是镁与空气中氧气等的反应.
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体.
【提出问题】黄色固体是什么呢?
【查阅资料】①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝.
【做出猜想】黄色固体是Mg3N2
【实验探究】请设计实验,验证猜想
| 实验操作 | 实验现象 | 结论 |
| 取少量黄色固体于试管中,加入 适量的水,并将并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试 纸变蓝 | 证明猜想正确 |
9.下列有关说法中正确的是( )
| A. | 钙、铁是人体中不可缺少的常量元素 | |
| B. | 金属活动性顺序表是金属活动性的判断依据 | |
| C. | 从元素周期表中可以确定该元素在自然界中的含量 | |
| D. | 碱和盐中一定含有金属元素 |
16.下列生产、生活中的变化,属于化学变化的是( )
| A. |  冰雪融化 | B. |  燃料燃烧 | C. |  泥水过滤 | D. |  风力发电 |
13.下列实验现象描述正确的是( )
| A. | 红磷在空气中燃烧,发出黄白色火焰,产生浓厚白色烟雾,放热,生成一种白色固体 | |
| B. | 电解水时电极两端具有气泡产生,且正极负极收集到的氧气与氢气的体积比为1:2 | |
| C. | 铜片插入硝酸银溶液中,紫红色固体表面覆盖一层银白色物质,溶液由蓝色变为无色 | |
| D. | 向盛有氢氧化镁的试管中滴入无色酚酞溶液,无明显现象 |
11.根据如表数据,回答问题.
(1)20℃时KNO3的溶解度是31.6g;
(2)60℃时,200gKNO3溶液中含溶质 100g,将该溶液降温至 20℃,可析出KNO368.4g;
(3)NaCl溶液中含有少量KNO3,提纯NaCl,采用的方法是蒸发结晶(选填“蒸发结晶”或“降温结晶”).
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 25.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
(2)60℃时,200gKNO3溶液中含溶质 100g,将该溶液降温至 20℃,可析出KNO368.4g;
(3)NaCl溶液中含有少量KNO3,提纯NaCl,采用的方法是蒸发结晶(选填“蒸发结晶”或“降温结晶”).
 图A是某元素在元素周期表中的相关信息,B是其原子结构示意图.
图A是某元素在元素周期表中的相关信息,B是其原子结构示意图.