题目内容
1.10g金属混合物与足量稀硫酸充分反,产生的氢气质量为1g,则该化合物的化学式为( )| A. | Fe Zn | B. | Zn Cu | C. | Al Cu | D. | Mg Zn |
分析 分别求出生成1克氢气需要金属的质量,必须一个质量大于10克,另一个质量小于10克,只有这样的混合物才符合条件.写出一个公用的化学方程式.
解答 解:解:设金属元素的符号是A,相对原子质量是B,在化合物中的化合价是X,金属的质量为m.
2A+XH2SO4═A2(SO4)X+XH2↑
2B 2X
m 2
$\frac{2B}{x}$=$\frac{2X}{1}$
m=$\frac{B}{X}$g
所以生成1克氢气所需要的金属的质量分别是:镁是12克;铝是9克;铁是28克;锌是32.5克;
所以该化合物是铝和铜的混合物,故选:C.
点评 学会使用这种方法,尤其适合选择题,注意铁和稀硫酸反应生成硫酸亚铁,即铁在化合物中的化合价是+2价.

练习册系列答案
相关题目
12.化学实验中,药品和仪器的存放应符合一定的规范.下列物质存放在对应的容器中,符合规范的是( )
| A. |  碳酸钙固体 | B. | 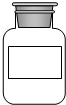 氢氧化钠溶液 | C. | 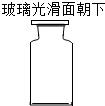 二氧化碳 | D. | 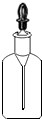 稀盐酸溶液 |
16.下列四组实验中的操作均能达到实验目的是 ( )
| 选项 | 实验目的 | 操作1 | 操作2 |
| A | 区分硝酸铜溶液和硝酸银溶液 | 观察颜色 | 加铁片 |
| B | 区分软水和硬水 | 加入肥皂水 | 过滤 |
| C | 区分氯化钙和碳酸钙固体 | 加水 | 加稀盐酸 |
| D | 区分黄铜(铜锌合金)和黄金 | 观察颜色 | 加稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
6. 青少年每天需摄取足量的蛋白质以保证正常的生长发育.
青少年每天需摄取足量的蛋白质以保证正常的生长发育.
(1)已知蛋白质中氮元素的平均质量分数为16%,下表是几种常见食物中的蛋白质含量:
如图是某学生早餐摄入的食物,请计算早餐所摄入的蛋白质中氮元素的质量(写出计算过程)
(2)蛋白质经体内进行新陈代谢后的主要产物是尿素(假设其他代谢产物不含氮元素),则尿素[CO(NH2)2]中碳元素与氧元素的质量比(最简整数比)为3:4.当人体代谢含5g氮元素的蛋白质时,请计算生成尿素的质量(写出计算过程).
 青少年每天需摄取足量的蛋白质以保证正常的生长发育.
青少年每天需摄取足量的蛋白质以保证正常的生长发育.(1)已知蛋白质中氮元素的平均质量分数为16%,下表是几种常见食物中的蛋白质含量:
| 食物 | 面粉 | 鸡蛋 | 瘦肉 | 牛奶 |
| 蛋白质含量 | 10% | 14% | 20% | 3% |
(2)蛋白质经体内进行新陈代谢后的主要产物是尿素(假设其他代谢产物不含氮元素),则尿素[CO(NH2)2]中碳元素与氧元素的质量比(最简整数比)为3:4.当人体代谢含5g氮元素的蛋白质时,请计算生成尿素的质量(写出计算过程).
11.将某盐酸与氢氧化钠溶液混合后,向其中滴加无色酚酞试液,溶液变红,下列说法正确的是( )
| A. | 混合后溶液中水的质量增大 | |
| B. | 混合后的溶液为氯化钠溶液 | |
| C. | 混合后的溶液中没有氢氧化钠 | |
| D. | 混合后的溶液中一定含有的溶质HCl |
 物质的溶解性如图为氯化钠、硝酸钠的溶解度曲线.
物质的溶解性如图为氯化钠、硝酸钠的溶解度曲线. 下列是金属或合金的性质或变化或应用,请根据题意填空:
下列是金属或合金的性质或变化或应用,请根据题意填空: 已知硝酸钾的溶解度随温度的升高而增大.如图甲,一块体积为V0的木块漂浮于60℃的硝酸钾
已知硝酸钾的溶解度随温度的升高而增大.如图甲,一块体积为V0的木块漂浮于60℃的硝酸钾