题目内容
在AgNO3和Fe(NO3)3的混合溶液中加入一定量的锌充分反应中,有少量金属析出,过滤后向滤液中滴加盐酸,有白色沉淀生成.则析出的金属是 .
考点:金属的化学性质,盐的化学性质
专题:金属与金属材料
分析:根据金属与盐反应的条件考虑本题,过滤后往滤液中滴加稀盐酸,有白色沉淀生成说明溶液中含有硝酸银,然后再具体分析问题即可.
解答:解:金属与盐反应的条件:①金属排在盐中金属的前面,②反应物中的盐溶于水,③金属钾、钙、钠除外.过滤后往滤液中滴加稀盐酸,有白色沉淀生成,说明溶液中含有银离子,所以剩余的固体必须是不能排在银的前面,否则继续与银离子反应,不可能有银离子剩余.所以析出的固体不会有铁、铜.只能是银.
故答案为:银.
故答案为:银.
点评:如果在溶液中有一种金属单质剩余,则排在该金属后面的金属阳离子不能存在.

练习册系列答案
相关题目
利用下列原理制取氧气,具有反应快、操作简便、能耗少、无污染的是( )
A、2H2O2
| ||||
B、2KClO3
| ||||
C、2H2O
| ||||
D、2HgO
|
下列元素属于非金属元素的是( )
| A、钾 | B、硅 | C、铜 | D、钠 |
在化学反应A+2B=C中,1.5克A与足量的B充分反应后,生成9.5克C,参加反应的B的质量为( )
| A、3克 | B、9.5克 |
| C、8克 | D、4克 |

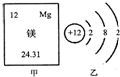 如图甲、乙所示是镁元素在元素周期表中的信息和镁原子的结构示意图,根据图示回答:
如图甲、乙所示是镁元素在元素周期表中的信息和镁原子的结构示意图,根据图示回答: