题目内容
12.某粗盐固体样品中含有少量CaCl2、MgCl2、Na2SO4、MgSO4和泥沙,进行以下操作可得到纯净的NaCl晶体:①加过量的NaOH溶液;②加H2O溶解;③加过量的BaCl2溶液;④过滤;⑤蒸发;⑥加过量的Na2CO3溶液;⑦加适量的稀盐酸,则正确的操作顺序是( )| A. | ②③①⑥④⑦⑤ | B. | ②①⑥③④⑦⑤ | C. | ①⑥②③④⑤⑦ | D. | ②①③⑥⑦④⑤ |
分析 从离子的角度分析粗盐中的杂质可知:溶液中的杂质离子为钙离子、镁离子、和硫酸根离子,根据镁离子用氢氧根离子沉淀,硫酸根离子用钡离子沉淀,钙离子用碳酸根离子沉淀,过滤要放在所有的沉淀操作之后,加碳酸钠要放在加氯化钡之后以便除去多余的钡离子.最后再用盐酸处理溶液中过量的碳酸根离子和氢氧根离子进行分析.
解答 解:首先要把粗盐溶于水形成溶液,然后镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,即⑥在③之后,排除B、C选项,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,最后经蒸发操作得到较纯净的氯化钠,D选项不应该在过滤之前加入稀盐酸,所以正确的选项是A.
故选A
点评 本题主要考查了在粗盐提纯中的物质的除杂或净化操作,在解此类题时,首先要了解需要除去的是哪些离子,然后选择适当的试剂进行除杂,在除杂质时,杂质和所加的试剂的状态一样,就要注意,加入的量的控制.

练习册系列答案
相关题目
3.下列有关说法正确的是( )
| A. | 常温下,过氧化氢溶液极易分解产生氧气 | |
| B. | 验满氧气的方法是用带火星的木条靠近集气瓶口 | |
| C. | 配制一定质量分数的NaCl溶液必需的玻璃仪器只有烧杯和玻棒 | |
| D. | 露置在空气中的氢氧化钠,其成分不会发生变化 |
20.为验证甲、乙、丙三种金属的活动性顺序,把三种金属分别放入稀盐酸中,只有乙表面无明显变化,把甲放入丙的硝酸盐溶液中,甲的表面有丙析出,则甲、乙、丙三种金属的活动性顺序由强到弱的是( )
| A. | 丙 甲 乙 | B. | 甲 丙 乙 | C. | 乙 甲 丙 | D. | 丙 乙 甲 |
7.决定元素种类的是( )
| A. | 中子数 | B. | 最外层电子数 | C. | 核外电子数 | D. | 质子数 |
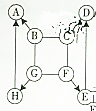 如图所示,A-H是初中化学常见的物质,图中“→”表示一种物质能转化为另一种物质,“-”表示两种物质能发生反应(部分反应物、生成物及反应条件未示出).其中A、G为常见的金属,E、H常温下为气体,E能形成温室效应,D常温下为液体,C是一种碱,在生活中可用来去除油污.请根据图填写下列空格:
如图所示,A-H是初中化学常见的物质,图中“→”表示一种物质能转化为另一种物质,“-”表示两种物质能发生反应(部分反应物、生成物及反应条件未示出).其中A、G为常见的金属,E、H常温下为气体,E能形成温室效应,D常温下为液体,C是一种碱,在生活中可用来去除油污.请根据图填写下列空格: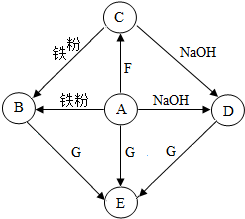 A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.
A-G是初中化学常见物质.其中,A的浓溶液能挥发出刺激性气味的气体,从C→D的反应过程中有蓝色沉淀生成,E为白色沉淀.如图是这些物质的转化关系,部分反应物、生成物及反应条件已省略.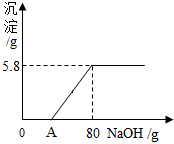 向盛有200g稀盐酸溶液的烧杯中加入一定量的铁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示,请回答:
向盛有200g稀盐酸溶液的烧杯中加入一定量的铁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示,请回答: