题目内容
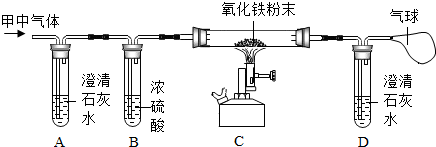
11.根据下列实验装置图,按要求回答下列问题:
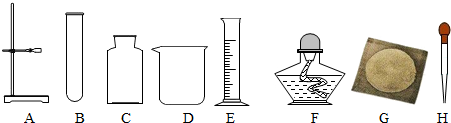
(1)仪器a的名称:集气瓶.
(2)实验室用高锰酸钾制取氧气,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,用此方法制备并且要收集较纯净的氧气应选用的发生和收集装置是AE(填字母序号).
(3)小明同学用F装置验证二氧化碳的性质.
①当通入二氧化碳一段时间后,试管①中产生的现象是紫色石蕊试液变红,说明二氧化碳能与水反应,此反应的化学方程式为H2O+CO2=H2CO3;试管②中的澄清石灰水变浑浊.
②G中观察到蜡烛由低到高依次熄灭,说明二氧化碳具有的性质是密度比空气大,且不能燃烧也不能支持燃烧,若两支蜡烛几乎同时熄灭,可能的原因是倾倒二氧化碳的速度过快(“倾倒时集气瓶的开口太大”、“蜡烛火焰高低距离太近”等符合要求的答案均可)(答一点即可).
分析 (1)据常用仪器回答;
(2)据反应原理书写方程式,该反应属于固体加热型,故选发生装置A,收集纯净的氧气用排水法;
(3)①二氧化碳能与水反应生成碳酸,碳酸可使石蕊变红,二氧化碳通入澄清的石灰水变浑浊;
②据现象可知:二氧化碳密度比空气大且不能燃烧、不支持燃烧,若两支蜡烛几乎同时熄灭,说明二者几乎同时接触到二氧化碳,据此结合实验分析解答.
解答 解:(1)标号仪器是收集气体的集气瓶;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,该反应属于固体加热型,故选发生装置A,收集纯净的氧气用排水法;
(3)①向石蕊试液中通入二氧化碳一段时间后,会观察到石蕊试液变红,因为二氧化碳可与水反应生成碳酸,碳酸使石蕊变红,反应方程式是:H2O+CO2=H2CO3;试管②中的澄清石灰水会变浑浊,因为二氧化碳与氢氧化钙反应生成不溶性的碳酸钙沉淀;
②G中观察到蜡烛由低到高依次熄灭,说明二氧化碳密度比 空气大,不能燃烧且不能支持燃烧;若两支蜡烛几乎同时熄灭,有可能是倾倒二氧化碳的速度过快,两支蜡烛几乎同时接触到二氧化碳,也可能是两支蜡烛火焰高低距离太近等;
故答案为:(1)集气瓶;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑; AE;
(3)①紫色石蕊试液变红; 水; H2O+CO2=H2CO3;变浑浊;
②密度比空气大,且不能燃烧也不能支持燃烧; 倾倒二氧化碳的速度过快(“倾倒时集气瓶的开口太大”、“蜡烛火焰高低距离太近”等符合要求的答案均可).
点评 本题主要考查制取氧气的反应原理、二氧化碳的性质,据反应物状态和反应条件选择发生装置,收集较纯净的气体通常用排水法,并能据实验现象灵活解答.

| A. | 滤渣中一定含有Ag、Fe | B. | 滤液中一定含有Fe2+、Al3+ | ||
| C. | 滤渣中一定含有Fe | D. | 滤液中一定含有Al3+、Ag+、Fe2+ |
| A. | 都不需要对气体发生装置加热 | |
| B. | 排空气法集气时都可以用燃着的木条验满 | |
| C. | 都可用排水法收集气体 | |
| D. | 都可以用相同的发生装置 |
| A. | 生活常识 | B. | 安全常识  | ||
| C. | 节约意识 | D. | 环保意识 |
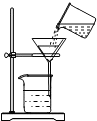 某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未,搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问:
某同学将浑浊的湖水样品倒入烧杯中,先加入明矾粉未,搅拌溶解,静置一会儿后,采用如图所示装置进行过滤,请问: