题目内容
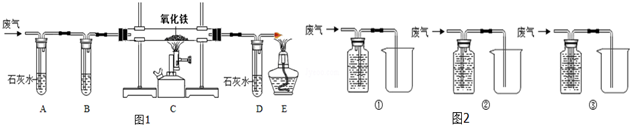
8.A、B、C、D、E是初中化学中常见的化合物,其中A为白色固体,B为无色气体,E为不溶于稀硝酸的白色沉淀,它们的关系如图所示.
请回答下列问题:
(1)白色沉淀E为AgCl;
(2)若现象I为“生成白色沉淀”,则A的化学式可能为BaCO3(写出一种即可);反应①的化学方程式为BaCO3+2HCl═BaCl2+H2O+CO2↑,反应②的化学方程式为BaCl2+H2SO4═BaSO4↓+2HCl;
(3)若现象I为“无明显变化”,则A的化学式可能为Na2CO3或K2CO3等.
分析 根据A、B、C、D、E是初中化学中常见的化合物,A为白色固体,B为无色气体,E为不溶于稀硝酸的白色沉淀,C和硝酸银反应水生成E,所以E是氯化银,C和稀硫酸反应会产生现象I,所以C中含有氯离子,可能含有硫酸根离子,A和稀盐酸反应生成三种物质,所以A是碳酸盐,B是二氧化碳,D是水,然后将推出的物质进行验证即可.
解答 解:A、B、C、D、E是初中化学中常见的化合物,A为白色固体,B为无色气体,E为不溶于稀硝酸的白色沉淀,C和硝酸银反应水生成E,所以E是氯化银,C和稀硫酸反应会产生现象I,所以C中含有氯离子,可能含有硫酸根离子,A和稀盐酸反应生成三种物质,所以A是碳酸盐,B是二氧化碳,D是水,经过验证,推导正确,所以
(1)白色沉淀E为AgCl;
(2)不溶于硝酸的白色沉淀有氯化银沉淀或硫酸钡沉淀,若现象I为“生成不溶于稀硝酸的白色沉淀”,加入的是硫酸所以不溶于硝酸的白色沉淀是硫酸钡沉淀,所以B是带钡离子的物质,即A中含有钡元素,因为A与盐酸反应生成三种物质,且D是二氧化碳,所以A是一种碳酸盐,所以A是碳酸钡;反应①的反应物是碳酸钡和盐酸,生成物是氯化钡、水、二氧化碳,化学方程式为:BaCO3+2HCl═BaCl2+H2O+CO2↑;
反应②是氯化钡与硫酸反应生成硫酸钡沉淀和盐酸,化学方程式为:BaCl2+H2SO4═BaSO4↓+2HCl;
(3)只要是生成的B与硫酸不反应或反应后现象不明显即可,所以A可以是Na2CO3或K2CO3.
故答案为:(1)AgCl;
(2)BaCO3,BaCO3+2HCl═BaCl2+H2O+CO2↑,BaCl2+H2SO4═BaSO4↓+2HCl;
(3)Na2CO3,K2CO3.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案| A. | 防止“白色污染”,就不能使用塑料制品 | |
| B. | 用脱硫煤作燃料,可减少温室效应 | |
| C. | 汽油中加入乙醇可节省石油资源,减少污染 | |
| D. | 废旧电池只要埋入土中,就能防止其对水源的污染 |
| A | 化学之最 | B | 符号中数字“2”的意义 |
| 地壳中含量多的金属元素:Fe 人体中含量最多的金属元素:Ca 空气中性质最稳定的物质:N2 | 2O:两个氧分子 $\stackrel{-2}{O}$:一个氧离子带两个单位负电荷 O2:两个氧原子 | ||
| C | 化学记录 | D | 物质及其应用 |
| 托盘天平可称质量为3.62g的食盐 筒量可量取9.26mL水 pH试纸测纯碱溶液pH为12.3 | 一氧化碳可用于炼铁 食盐可作保存食品的防腐剂 碳酸氢钠可作面食发酵粉起泡剂 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 氢气燃烧 | B. | 干冰升华 | C. | 滴水成冰 | D. | 石油的分馏 |
| 反应时间t/s | t1 | t2 | t3 | t4 |
| 反应后固体的质量m/g | 6 | 4.8 | 2 | 2 |
(2)生成二氧化碳的质量.
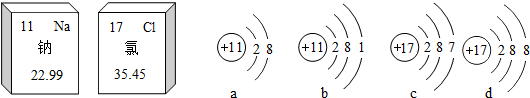
| A. | 钠、氯都属于金属元素 | B. | 氯化钠是由a,d两种粒子构成的 | ||
| C. | 氯的相对原子质量是35.45g | D. | a表示的是一种阴离子 |
| A. |  塑料保鲜膜 | B. |  纯棉毛巾 | C. |  真丝围巾 | D. |  不锈钢锅 |
| A. | 专指物质跟氧气发生的反应 | B. | 指物质跟氧发生的反应 | ||
| C. | 氧化反应的产物只有一种 | D. | 氧化反应一定是化合反应 |