题目内容
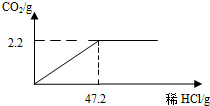 某化学兴趣小组的同学采集了一些大理石样品,为了测定样品中碳酸钙的质量分数,取样品8g粉碎成粉末置于烧杯中,向其中加入一定质量分数的稀盐酸并不断搅拌,反应的关系如图所示:
某化学兴趣小组的同学采集了一些大理石样品,为了测定样品中碳酸钙的质量分数,取样品8g粉碎成粉末置于烧杯中,向其中加入一定质量分数的稀盐酸并不断搅拌,反应的关系如图所示:(1)计算样品中碳酸钙的质量分数.
(2)计算恰好完全反应时所得溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:根据图中数据可以判断生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量和生成的氯化钙的质量,进一步可以计算样品中碳酸钙的质量分数和所恰好完全反应时所得溶液中溶质的质量分数.
解答:解:根据图中数据可以判断生成二氧化碳的质量为2.2g
设碳酸钙的质量为x,生成中氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
x y 2.2g
=
=
x=5g
y=5.55g
(1)样品中碳酸钙的质量分数
×100%=75%
(2)恰好完全反应时所得溶液中溶质的质量分数
×100%=11.1%
答案:
(1)样品中碳酸钙的质量分数75%
(2)恰好完全反应时所得溶液中溶质的质量分数11.1%
设碳酸钙的质量为x,生成中氯化钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 111 44
x y 2.2g
| 100 |
| x |
| 111 |
| y |
| 44 |
| 2.2g |
x=5g
y=5.55g
(1)样品中碳酸钙的质量分数
| 5g |
| 8g |
(2)恰好完全反应时所得溶液中溶质的质量分数
| 5.55g |
| 5g+47.2g-2.2g |
答案:
(1)样品中碳酸钙的质量分数75%
(2)恰好完全反应时所得溶液中溶质的质量分数11.1%
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
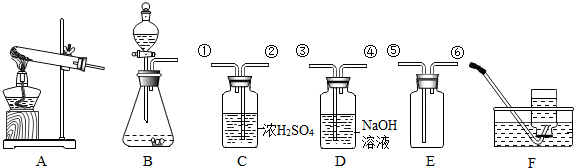
实验室制取时CO2,应选用的仪器组为( )
| A、漏斗、集气瓶、水槽、导管 |
| B、酒精灯、试管、导管、漏斗 |
| C、平底烧瓶、长颈漏斗、集气瓶、导管 |
| D、集气瓶、酒精灯、导管、水槽 |
下列变化与其他变化有本质不同的是( )
| A、实验室用双氧水制氧气 |
| B、工业制氧气 |
| C、光合作用产生氧气 |
| D、实验室用高锰酸钾制氧气 |
下列物质属于纯净物的是( )
| A、空气 | B、生理盐水 |
| C、部分结冰的水冰 | D、稀有气体 |
在t℃时,将120g氯化钠溶液蒸发掉10g水时有2.5g晶体析出,再蒸发掉10g水时有3.6g晶体析出,若继续蒸发掉10g水,将析出晶体( )
| A、10g | B、8g |
| C、7.5g | D、3.6g |