题目内容
10.逻辑推理是化学学习中常用的思维方法,以下推理正确的是( )| A. | 中和反应有盐和水生成,因此生成盐和水的反应都是中和反应 | |
| B. | 碱溶液的pH大于7,因此pH大于7的溶液一定是碱溶液 | |
| C. | 稀有气体元素的原子最外层电子数为8(氦为2),因此微粒 一定是稀有气体元素的原子 一定是稀有气体元素的原子 | |
| D. | 酒精完全燃烧生成二氧化碳和水的分子个数比为2:3,因此推出酒精分子中碳、氢原子个数比为1:3 |
分析 A.根据中和反应的概念解答;
B.有些盐类显碱性.例如碳酸钠溶液;
C.根据原子最外层电子数为8(氦除外)的微粒可能一原子阳离子或阴离子解答.
D.根据质量守恒定律来分析.
解答 解:A.中和反应生成盐和水,但是生成盐和水的反应不都是中和反应,例如氢氧化钠和二氧化碳反应生成碳酸钠和水,不是中和反应,故错误;
B.pH大于7的溶液不一定是碱的溶液,也可能是某些盐的溶液,例如碳酸钠的溶液呈碱性,属于盐类物质,故错误;
C.原子最外层电子数为8(氦除外)的微粒可能是原子、阳离子或阴离子,因此微粒 不一定是稀有气体元素的原子,故错误;
不一定是稀有气体元素的原子,故错误;
D.一个二氧化碳分子中含有1个碳原子,1个水分子中含有2个氢原子,所以二氧化碳和水的分子个数比为2:3时,碳原子与氢原子的个数比为2:6=1:3,而由质量守恒定律可知,反应前后原子的种类和数目不变,因此推出酒精分子中碳、氢原子个数比为1:3,故正确.
故选D.
点评 本题考查的是对常见的概念、理论的推理,完成此题,可以依据已有的知识进行.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目
2.下列除杂方案中最合理的是( )
| A. | 用点燃的方法除掉二氧化碳中混有的少量一氧化碳 | |
| B. | 加入过量的稀盐酸除掉氧化钙中的少量碳酸钙 | |
| C. | 除掉硫酸锌溶液中少量硫酸亚铁--加入过量的锌粉并过滤 | |
| D. | 除掉镁粉中少量铁粉可以加入足量的稀硫酸并过滤 |
4.下列反应不属于置换反应的是( )
| A. | 3H2+Fe2O3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe+3H2O | B. | Fe+2HCl═FeCl2+H2↑ | ||
| C. | Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | D. | 3Fe+4H2O$\frac{\underline{\;\;△\;\;}}{\;}$4H2+Fe3O4 |
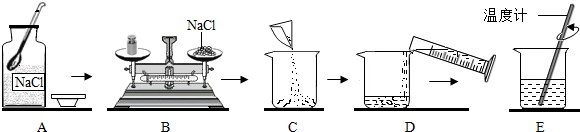
19.如图所示是实验过程中的部分操作,其中正确的是( )
| A. | 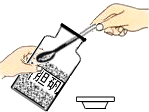 取一定量粗盐 取一定量粗盐 | B. | 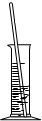 溶解 | C. | 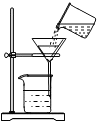 过滤 | D. |  蒸发结晶 |
15.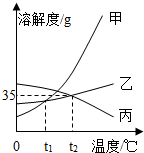 已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:
已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:
(1)依据表格数据,绘制出氯化钾和硝酸钾的溶解度曲线如图所示,图中能表示硝酸钾的溶解度曲线的是甲(选填“甲”或“乙”).
(2)t2℃时,丙物质的溶解度为35g.现有该温度下接近饱和的丙物质的溶液,使其变成饱和溶液,可采用的方法有加入丙(或恒温蒸发溶剂).
(3)40℃时,将30g氯化钾放入盛有50g水的烧杯中,充分溶解后,所得溶液的质量为70g.此时,该溶液的溶质质量分数为28.6%(结果精确到0.1%).若将烧杯内的物质降温到20℃,溶液中不变的是B(填写序号)
A、溶质的质量 B、溶剂的质量 C、溶液的质量 D、溶质质量分数.
 已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:
已知氯化钾和硝酸钾在不同温度时的溶解度如表所示:| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | 氯化钾 | 27.6 | 34.0 | 40.0 | 45.5 |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110.0 | |
(2)t2℃时,丙物质的溶解度为35g.现有该温度下接近饱和的丙物质的溶液,使其变成饱和溶液,可采用的方法有加入丙(或恒温蒸发溶剂).
(3)40℃时,将30g氯化钾放入盛有50g水的烧杯中,充分溶解后,所得溶液的质量为70g.此时,该溶液的溶质质量分数为28.6%(结果精确到0.1%).若将烧杯内的物质降温到20℃,溶液中不变的是B(填写序号)
A、溶质的质量 B、溶剂的质量 C、溶液的质量 D、溶质质量分数.
2.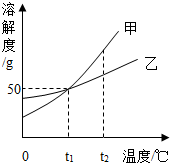 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
 如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )
如图是甲、乙两种固体物质(不含结晶水)的溶解度曲线,下列叙述错误的是( )| A. | t1℃时,甲、乙两种物质的溶解度都是50g | |
| B. | t2℃时,在等质量甲、乙两种溶液中,甲中溶质的质量一定大于乙 | |
| C. | t1℃时,将甲、乙的饱和溶液升温至t2℃,二者溶质的质量分数相等 | |
| D. | 甲溶液中含有少量乙,可以用冷却热饱和溶液的方法提纯甲 |
20.下列括号中对日常生活的变化判断正确的是( )
| A. | 水蒸发(化学变化) | B. | 鞭炮爆炸(化学变化) | ||
| C. | 食物腐烂(物理变化) | D. | 烧鱼时把鱼烧焦(物理变化) |