题目内容
8.计算:取NaCl和Na2CO3的混合物20g,加入100g水充分溶解,向其中加入100g稀盐酸恰好完全反应,反应结束后,测得反应后溶液的总质量为215.6g,求稀盐酸中溶质的质量分数.分析 碳酸钠与稀盐酸反应生成氯化钠、水和二氧化碳;由质量守恒定律,混合物减少的质量即为生成二氧化碳气体的质量,由反应的化学方程式列式计算出参加反应的稀盐酸中溶质的质量,进而计算出稀盐酸中溶质的质量分数.
解答 解:由质量守恒定律,生成二氧化碳的质量为20g+100g=100g-215.6g=4.4g
设参加反应的稀盐酸中溶质的质量为x
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73 44
x 4.4g
$\frac{73}{44}=\frac{x}{4.4g}$ x=7.3g
稀盐酸中溶质的质量分数为$\frac{7.3g}{100g}$×100%=7.3%.
答:稀盐酸中溶质的质量分数为7.3%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的前提和关键.

练习册系列答案
 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
19.下列实验操作正确的是( )
| A. |  收集氧气 | B. | 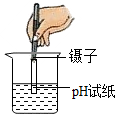 测定溶液的pH | C. |  添加酒精 | D. | 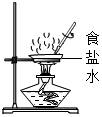 蒸发食盐水 |
16.某化学课外活动小组欲测定一瓶部分变质的熟石灰样品中Ca(OH)2的质量分数,取0.5g样品,加足量水使之充分溶解,搅拌过滤后,在滤液中加入10%盐酸溶液,加入盐酸溶液的质量和溶液的pH关系见表.
求该样品中Ca(OH)2的质量分数.(写出计算过程)
| 加入盐酸溶液的质量/g | 0 | 2.5 | 3.65 | 6 |
| 溶液的pH | 12 | 11 | 7 | 2 |
9.物质的性质决定物质的用途.下列物质的用途是由其物理性质决定的是( )
| A. | 氢气作高能燃料 | B. | 氧气用于医疗急救 | ||
| C. | 铜丝作导线 | D. | 氧气用于焊接金属 |
10. 某化学实验室产生的废液中含有FeCl2、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
某化学实验室产生的废液中含有FeCl2、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
 某化学实验室产生的废液中含有FeCl2、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )
某化学实验室产生的废液中含有FeCl2、CuCl2、BaCl2三种物质,现设计下列方案对废液进行处理,以回收金属并制备氯化钡、氯化铁晶体下列说法不正确的是( )| A. | 沉淀I中的单质为铁和铜 | |
| B. | 氧化方程式为2FeCl2+H2O2+HCl═2FeCl3+2H2O | |
| C. | “过滤3”到“氧化”是为了充分回收铁元素 | |
| D. | 试剂X应为NaOH |
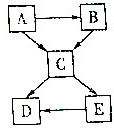 现有A~E五种常见物质,且都含有同一种非金属元素,其中E广泛用于洗涤剂的生产,它们的转化关系如图,请回答:
现有A~E五种常见物质,且都含有同一种非金属元素,其中E广泛用于洗涤剂的生产,它们的转化关系如图,请回答: