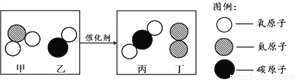
��Ŀ����
���ճ�����������������ȷ����( )
A .������Ĵ���ʯ���������գ������ý�����
B.����ˮ���Բ������������ֱ������ϴ������
C.���ڵ����Ż������ˮ���
D.���������ƴ���ʳ�γ���
D ��������A��������Ĵ���ʯ��Ҫ�ɷ���̼��ƣ���������ԣ��ᷢ����ѧ��Ӧ���������ý�����������B������ˮ�������������ˡ�����������ɱ��������ֱ������ϴ�·�����ȷ��C�����ڵ����Ż�����ù��Ǹ��𣬲�����ˮ���Ҫ�ù��Ǹ��𣬴���D����Ϊ���������ж������й�ҵ�ε�ʳƷ������Σ���ܴ����°��ԣ��ʲ������������ƴ���ʳ�γ��ˣ�����ѡD��
��ϰ��ϵ�д�
 ���ĺ����Ͼ�������ϵ�д�
���ĺ����Ͼ�������ϵ�д�
�����Ŀ
���� 4 ��ͼ������ȷ��ӳ��Ӧ�仯��ϵ��( )
A | B | C | D |
|
|
|
|
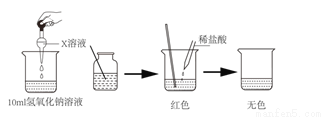
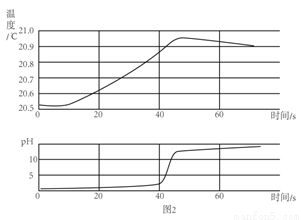
��һ����ϡ�����м� �� NaOH ��Һ | Ũ���᳤�ڱ�¶�ڿ� ���� | ��һ������������Һ ����ε����������� ��Һ������ | ��ͬ�����£������� ����ȵ����ݹ��壬a Ϊ����غͶ������� �Ļ���b Ϊ���� �� |
A. A B. B C. C D. D
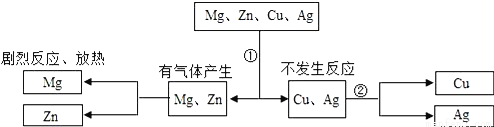
C ��������A���ڷ�Ӧ��ʼʱ��ϡ���ᡢNaOH��Һ�ж�����ˮ�������Һ��ˮ������������Ϊ0������B��Ũ���᳤�ڱ�¶�ڿ����У����տ����е�ˮ�����ʵ�����������С��������Ϊ0������C������������������Ӧ�������ᱵ������ˮ����һ������������Һ����ε����������� ��Һ����Һ�еĿ������ƶ���������Ŀ���ϼ��٣�������������ǡ����ȫ��Ӧʱ����Һ�м���û�п������ƶ������ӣ�������Ϊ0������������...ͨ��һ����ѧ��Ӧʵ����ͼ��ʾ��X��Y��Z�������ʼ�ת����������X��Y��Z��Ӧ�����ʲ���ʵ������ת������
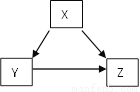
X | Y | Z | |
A | CO2 | Na2CO3 | CaCO3 |
B | CuO | Cu(NO3)2 | Cu(OH)2 |
C | HCl | BaCl2 | NaCl |
D | Mg | MgO | MgCl2 |
A. A B. B C. C D. D
B ��������������ѧ֪ʶ��������Ϣ֪��A.������̼ͨ������������Һ��������̼���ƣ�̼���ƺ��������Ʒ�Ӧ��������̼��ơ�B.����ͭ�����ᷴӦ����������ͭ������ͭ����һ������������ͭ��C.���������������Һ��Ӧ�������Ȼ������Ȼ�����̼���Ʒ�Ӧ������̼�ᱵ�������Ȼ��ơ�D.þ��������Ӧ����������þ������þ�����ᷴӦ�������Ȼ�þ��