题目内容
4.如图1是实验室所用盐酸试剂瓶上标签的部分内容,请仔细阅读后计算:
(1)欲配制14.3%的稀盐酸1000g,需要用这种盐酸多少毫升?
(2)取10g石灰石样品,与足量(1)中配制的稀盐酸反应测定出二氧化碳的质量与反应时间的关系图(如图2),试求样品中碳酸钙的质量分数.(其反应方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑,假设样品中其他杂质不参加反应)
分析 (1)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
(2)由反应放出二氧化碳的质量,根据反应的化学方程式计算参加反应的碳酸钙的质量,碳酸钙质量与样品的质量比可计算石灰石样品中碳酸钙的质量分数.
解答 解:(1)设需要用这种盐酸的体积为x,根据溶液稀释前后,溶质的质量不变,
则1000g×14.3%=1.1g/cm3×x×20% x=650cm3=650mL.
(2)根据图示可知:产生二氧化碳的质量为3.3g,设样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{x}=\frac{44}{3.3g}$
x=7.5g
样品中碳酸钙的质量分数=$\frac{7.5g}{10g}×$100%=75%
答案:
(1)需要用这种盐650毫升
(2)样品中碳酸钙的质量分数为75%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
15.现有镁、铝、锌的混合物20g与适量的稀硫酸恰好完全反应,蒸发水后得到固体68g,如果将实验中用的稀硫酸改为稀盐酸,其他操作不变,蒸发后得到固体的质量为( )
| A. | 68g | B. | 91g | C. | 55.5g | D. | 无法确定 |
15.下列是日常生活中常发生的一些变化,其中属于化学变化的一组是( )
| A. | 水受热沸腾,酒精挥发 | B. | 汽油挥发,动物的呼吸作用 | ||
| C. | 食物发霉,铁锅生锈 | D. | 工业制氧气,西瓜成汁 |
12.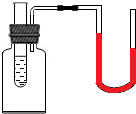 如图所示,小试管中盛有水和石蕊试液,U型管两侧内水面持平.向试管中加入某物质后,石蕊试液变红,且U型管两侧水面左低右高,则加入的物质为( )
如图所示,小试管中盛有水和石蕊试液,U型管两侧内水面持平.向试管中加入某物质后,石蕊试液变红,且U型管两侧水面左低右高,则加入的物质为( )
 如图所示,小试管中盛有水和石蕊试液,U型管两侧内水面持平.向试管中加入某物质后,石蕊试液变红,且U型管两侧水面左低右高,则加入的物质为( )
如图所示,小试管中盛有水和石蕊试液,U型管两侧内水面持平.向试管中加入某物质后,石蕊试液变红,且U型管两侧水面左低右高,则加入的物质为( )| A. | CaO | B. | NaOH | C. | 浓H2SO4 | D. | NaCl |
19.研究表明,缺碘会引起甲状腺肿大,可从海带中补碘.这里的“碘”是指( )
| A. | 原子 | B. | 分子 | C. | 离子 | D. | 元素 |
9.下列物质的用途中,主要应用其化学性质的是( )
| A. | 用铁铝制作饮具 | B. | 用干冰进行人工降雨 | ||
| C. | 用酒精作燃料 | D. | 用铜作导线 |
16.下列操作或说法正确的是( )
①用100mL量筒量取10mL水
②不慎将酒精洒在桌面上并燃烧,立即用湿抹布扑灭
③加热固体或液体时试管夹应从试管口套入并固定在距管口约$\frac{1}{3}$处
④某同学用托盘天平称得一支试管的质量为31.35g
⑤用试管加热物质时,试管内外壁均不得有水
⑥为防止液体滴在试管外,应将滴管伸入试管内滴加液体.
①用100mL量筒量取10mL水
②不慎将酒精洒在桌面上并燃烧,立即用湿抹布扑灭
③加热固体或液体时试管夹应从试管口套入并固定在距管口约$\frac{1}{3}$处
④某同学用托盘天平称得一支试管的质量为31.35g
⑤用试管加热物质时,试管内外壁均不得有水
⑥为防止液体滴在试管外,应将滴管伸入试管内滴加液体.
| A. | ② | B. | ②③⑤ | C. | ①②③⑤⑥ | D. | ②③④⑤ |
13.下列各微粒的示意图中,表示阴离子的是( )
| A. | 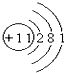 | B. |  | C. | 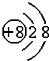 | D. |  |