题目内容
6.实验室制取气体是初中重要的一项实验,结合下列实验装置图回答有关问题:
(1)装置Ⅰ是加热固体的装置,改正其中的错误试管口应略低于试管底部(合理说法均可);如用改进后的装置制取氧气请写出化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑(或 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑);
(2)写出使用装置II制取CO2的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑;;
(3)写出装置Ⅳ中一种玻璃仪器名称集气瓶(或玻璃导管 );
(4)实验室制取氢气、氧气、二氧化碳等气体,既能用装置Ⅳ,又能用装置Ⅴ收集的气体有H2 (填化学式);
(5)用装置Ⅲ排空气法收集二氧化碳,则气体应从a(填“a”或“b”) 端进入;若用此装置来干燥二氧化碳则集气瓶中应装入浓硫酸.气体应从a(填“a”或“b”)端进入,此物质应具有吸水性 性.
(6)用浓盐酸与大理石在上述装置中反应,将制取的CO2通入紫色石蕊试液,发现紫色石蕊试液变红色,对可能造成这一现象的解释不合理的是A(填字母序号).
A.产生的CO2直接使石蕊试液变红剂
B.挥发出的氯化氢溶于水,使石蕊试液变红
C.产生的CO2与水反应生成碳酸,使石蕊试液变红.
分析 (1)加热固体时试管口应略低于试管底部,防止冷凝水倒流引起试管炸裂;A装置的特点适用于固体加热型的反应,可以选择高锰酸钾或氯酸钾加热制取氧气,据此书写化学方程式即可;
(2)装置II属于固液常温型,所以用来制取CO2的物质是稀盐酸和大理石或石灰石,据反应原理书写方程式;
(3)装置中集气瓶和导管均属于玻璃仪器;
(4)能用向下排空气法收集的气体密度比空气小,能用排水法收集的气体不溶于水或不易溶于水;
(5)二氧化碳密度比空气大,所以应从长管进气,将空气挤压到集气瓶上部排出;干燥气体要选择具有吸水性的物质,还得保证所加试剂不与待干燥气体发生反应;
(6)根据显酸性的溶液能使石蕊试液变红色进行分析.
解答 解:(1)加热固体时试管口应略低于试管底部,防止冷凝水倒流引起试管炸裂;A装置的特点适用于固体加热型的反应,可以选择高锰酸钾或氯酸钾加热制取氧气,反应的方程式为:2KClO$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑(或 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑);
(2)装置II属于固液常温型,用来制取CO2的物质是稀盐酸和大理石或石灰石,反应方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)装置中集气瓶和导管均属于玻璃仪器;
(4)能用向下排空气法收集的气体密度比空气小,能用排水法收集的气体不溶于水或不易溶于水,氧气、二氧化碳、氢气三种气体中只有氢气密度比空气小,可用向下排空气法收集,且氢气难溶于水,可用排水法收集;
(5)二氧化碳密度比空气大,所以应从长管进气,将空气挤压到集气瓶上部排出;干燥二氧化碳一般选择具有吸水性的浓硫酸,干燥气体时气体应从装置中的长管通入;
(6)产生的CO2与水反应生成碳酸,使石蕊溶液变红,挥发出的氯化氢溶于水,形成盐酸可使石蕊溶液变红,二氧化碳本身不能使石蕊变红,故A错误;
故答案为:(1)试管口应略低于试管底部(合理说法均可);
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)集气瓶(或玻璃导管 );
(4)H2;
(5)a;浓硫酸;a;吸水性;
(6)A.
点评 了解实验室制取气体时的注意事项,气体的收集方法,反应原理等知识,才能结合题意解答,要根据题意细心分析.

 提分百分百检测卷单元期末测试卷系列答案
提分百分百检测卷单元期末测试卷系列答案 小学期末标准试卷系列答案
小学期末标准试卷系列答案| A. | 二氧化碳 | B. | 氯化钠晶体 | C. | 氢气 | D. | 银 |
| A. | 都是黑色固体 | |
| B. | 在氧气中充分燃烧时都生成二氧化碳 | |
| C. | 物理性质相同 | |
| D. | 金刚石、石墨是碳单质,C60是碳的化合物 |
| A. | KCl | B. | CO(NH2)2 | C. | KNO3 | D. | Ca3(PO4)3 |
【探究实验一】碳酸氢钠溶液的酸碱性:用pH试纸测得碳酸氢钠溶液的pH约为10.由此得出的结论是碳酸氢钠溶液呈碱性.
【探究实验二】碳酸氢钠能否与酸反应:取少量固体放入试管中,滴加足量的稀盐酸,现象为产生大量气泡,固体逐渐溶解.结论:碳酸氢钠能与酸反应.
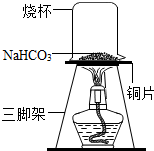
【探究实验三】碳酸氢钠的热稳定性:取一定量的碳酸氢钠放在铜片上加热,如图所示.
(1)加热一段时间后,观察到烧杯内壁有水珠.
(2)充分加热后,将烧杯迅速倒转过来,加入适量的澄清石灰水,震荡,观察到澄清石灰水变浑浊.
(3)通过进一步实验来确定充分加热后的固体产物的成分.限选试剂及仪器:稀盐酸、氯化钙溶液、澄清石灰水、酚酞溶液、蒸馏水、试管、胶头滴管
| 序号 | 实验操作 | 预期现象 | 结论 |
① | 取少量加热后的固体产物放入试管A中,加入适量蒸馏水,充分振荡溶解,滴加足量氯化钙溶液,振荡,静置. | 产生白色沉淀 | 产物含碳酸钠 |
| ② | 取操作①后的上层清液于试管B中,滴加酚酞试液. | 酚酞试液不变色 | 产物不含NaOH |
| 编 号 | 第 1 次 | 第 2次 | 第 3次 |
| 所取固体样品的质量/g | 13 | 10 | 10 |
| 样品用98g水溶解后,加入CaCl2溶液的质量/g | 100 | 100 | 125 |
| 反应后生成沉淀的质量/g | 8 | 8 | 8 |
①固体样品中氯化钠的质量分数是15.2%;
②第2次反应结束后溶液中溶质质量分数是多少?(写出必要的计算题过程)
| A. | 2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | B. | C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2 | ||
| C. | C2H5OH+3O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+3H2O | D. | S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2 |