题目内容
10. “见著知微,见微知著”是化学重要的思维方法.
“见著知微,见微知著”是化学重要的思维方法.(1)用微观粒子的观点解释,氯化氢由气态变为液态是因为氯化氢分子间的间隔变小了.
(2)以下是四种微观粒子的结构示意图
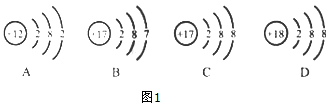
①表示Cl-的是C(填序号).
②由A的阳离子和C组成的化合物的名称是氧化镁;
B和C属于同种元素(填“原子”、“离子”或“元素”).
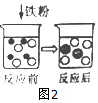
(3)如图2,表示盐酸与铁粉反应的示意图,图中“
 ”、“○”、“
”、“○”、“ ”各代表一种粒子,其中“
”各代表一种粒子,其中“ ”表示的是Fe2+(填符号)
”表示的是Fe2+(填符号)
分析 (1)根据分子间有间隔的特性分析回答;
(2)①根据粒子的结构示意图分析;
②根据元素的定义及组成的物质分析回答;
(3)根据铁与稀盐酸的反应分析回答.
解答 解:(1)用微观粒子的观点解释,氯化氢由气态变为液态是因为氯化氢分子间的间隔变小了.
(2)①由粒子的结构示意图可知,C的质子数是17,电子数是18,表示Cl-.
②由粒子的结构示意图可知,A的阳离子是镁离子,C是氯离子,构成的化合物的名称是氯化镁;B和C的质子数相同,属于同种元素.
(3)稀盐酸与铁反应生成了氯化亚铁和氢气,如图2,表示盐酸与铁粉反应的示意图,图中“ ”、“○”、“
”、“○”、“ ”各代表一种粒子,其中“
”各代表一种粒子,其中“ ”表示的是 Fe2+.
”表示的是 Fe2+.
故答为:(1)氯化氢分子间的间隔变小了.(2)①C;②氯化镁;元素.(3)Fe2+.
点评 了解原子结构示意图与离子结构示意图的区别和联系;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称.

练习册系列答案
相关题目
20.下列实验不能达到实验目的是( )
| A. | 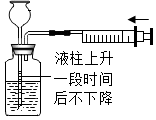 检查装置气密性 检查装置气密性 | B. | 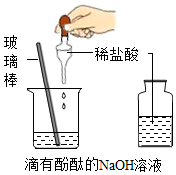 证明酸与碱能发生反应 证明酸与碱能发生反应 | ||
| C. | 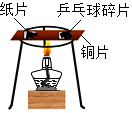 验证不同物质的着火点不同 验证不同物质的着火点不同 | D. | 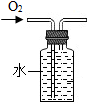 收集氧气 收集氧气 |
1.常用作焙制糕点的是( )
| A. | 氢气 | B. | 活性炭 | C. | 二氧化碳 | D. | 碳酸氢钠 |
5.某混合气体可能含有CO、CO2、CH4和HCl中的一种或几种,为了确定其成分,将混合气体按如图所示装置进行实验(假设各步均充分反应或吸收),结果装置A中澄清的石灰水不变浑浊,但混合气体的体积明显减小;装置D增重1.8g;装置E增重2.2g,下列关于该混合气体成分的分析中,错误的是( )

| A. | 一定不含CO2,一定含HCl | B. | 一定含CH4、一定不含CO | ||
| C. | 可能只含CH4和HCl | D. | 可能含CO2 |
15.下列化学用语表示正确的是( )
| A. | 一个水分子:H2O | |
| B. | 氢气:He | |
| C. | 一个钙离子:Ca+1 | |
| D. | 二氧化硅中硅元素的化合价:$\stackrel{4+}{Si{O}_{2}}$ |
2.A、B在不同温度的溶解度数据如表,请回答下列问题:
(1)A、B溶解度相等的温度在20-40℃之间.
(2)A中混有少量的B,想要得到纯净的A的方法是冷却热饱和溶液.
(3)在60℃时,将20gB加入到50g水中,充分溶解后降温到20℃,所得溶液的溶质质量分数为26.5%.
| 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | |
| A | 13.3g | 31.6g | 63.9g | 110g | 169g |
| B | 35.7g | 36g | 36.6g | 37.3g | 3.4g |
(2)A中混有少量的B,想要得到纯净的A的方法是冷却热饱和溶液.
(3)在60℃时,将20gB加入到50g水中,充分溶解后降温到20℃,所得溶液的溶质质量分数为26.5%.
19.下列有关溶液的说法正确的是( )
| A. | 均一、稳定的无色液体一定是溶液 | |
| B. | 消毒用的医用碘酒中溶质是碘,溶剂是酒 | |
| C. | 常温下饱和的澄清石灰水升高温度会变浑浊 | |
| D. | 20℃时氯化钠溶解度是36g,说明20℃时100g氯化钠饱和溶液中溶有36g氯化钠 |
16.下列物质中属于纯净物的是( )
| A. | 洁净的空气 | B. | 糖水 | C. | 红磷 | D. | 海水 |