题目内容
用125g石灰石样品与稀盐酸反应(CaCO3+2HCl═CaCl2+CO2↑+H2O),产生气体体积与加入稀盐酸的质量关系如图所示.(1)反应结束时,生成二氧化碳的体积是______L,这些CO2的质量为______ g(结果取整数,CO2的密度为1.97g/L);
(2)求该石灰石样品中CaCO3的质量分数.

【答案】分析:利用碳酸钙与盐酸反应生成气体的质量,再根据化学方程式可以计算出样品中碳酸钙的质量,再根据: ×100%,就能计算出石灰石样品中碳酸钙的质量分数.
×100%,就能计算出石灰石样品中碳酸钙的质量分数.
解答:解:(1)由图可知反应结束时,生成二氧化碳的体积是22.4L,CO2的质量=22.4L×1.97g/L=44g.
设25g石灰石样品中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 44g
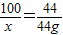
x=100g
石灰石样品中CaCO3的质量分数为: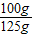 ×100%=80%
×100%=80%
答:该石灰石样品中CaCO3的质量分数为80%.
故答案为:
(1)22.4;44;
(2)80%.
点评:本题主要考查根据化学方程式的计算,难度较小.石灰石为混合物,石灰石中除了碳酸钙之外还有杂质,不能将石灰石的质量直接代入化学方程式进行计算.
 ×100%,就能计算出石灰石样品中碳酸钙的质量分数.
×100%,就能计算出石灰石样品中碳酸钙的质量分数.解答:解:(1)由图可知反应结束时,生成二氧化碳的体积是22.4L,CO2的质量=22.4L×1.97g/L=44g.
设25g石灰石样品中CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 44g
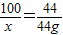
x=100g
石灰石样品中CaCO3的质量分数为:
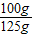 ×100%=80%
×100%=80%答:该石灰石样品中CaCO3的质量分数为80%.
故答案为:
(1)22.4;44;
(2)80%.
点评:本题主要考查根据化学方程式的计算,难度较小.石灰石为混合物,石灰石中除了碳酸钙之外还有杂质,不能将石灰石的质量直接代入化学方程式进行计算.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
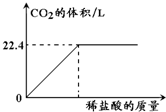 用125g石灰石样品与稀盐酸反应(CaCO3+2HCl═CaCl2+CO2↑+H2O),产生气体体积与加入稀盐酸的质量关系如图所示.
用125g石灰石样品与稀盐酸反应(CaCO3+2HCl═CaCl2+CO2↑+H2O),产生气体体积与加入稀盐酸的质量关系如图所示.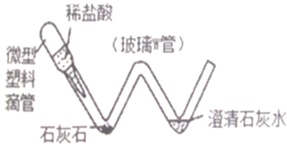 某化学兴趣小组设计了一套微型实验装置,用来测定一种石灰石样品中碳酸钙的质量数分数,具体做法是:
某化学兴趣小组设计了一套微型实验装置,用来测定一种石灰石样品中碳酸钙的质量数分数,具体做法是: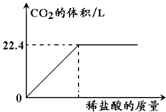 用125g石灰石样品与稀盐酸反应(CaCO3+2HCl═CaCl2+CO2↑+H2O),产生气体体积与加入稀盐酸的质量关系如图所示.
用125g石灰石样品与稀盐酸反应(CaCO3+2HCl═CaCl2+CO2↑+H2O),产生气体体积与加入稀盐酸的质量关系如图所示.