题目内容
6.写出反应的化学方程式:(1)分解反应:KMnO42KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
KClO32KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑
H2O22H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
H2O2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑
H2CO3H2CO3=H2O+CO2↑
CaCO3CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑
(2)置换反应:(至少写一个方程式)
金属单质+酸--盐+氢气Mg+2HCl=MgCl2+H2↑
金属单质+盐--新盐+新金属Fe+CuSO4=Cu+FeSO4
氢气+金属氧化物H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O
碳+金属氧化物C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)高锰酸钾在加热的条件下分解为锰酸钾、二氧化锰和氧气,故填:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
氯酸钾在二氧化锰的催化作用下加热分解为氯化钾和氧气,故填:2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑;
过氧化氢在二氧化锰的催化作用下生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
水在通电条件下生成氢气和氧气,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.故答案为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
碳酸分解为水和二氧化碳,故填:H2CO3=H2O+CO2↑;
碳酸钙在高温的条件下分解为氧化钙和二氧化碳,故填:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(2)活泼金属与酸发生置换反应生成盐和氢气,如镁和稀盐酸反应生成氯化镁和氢气,故填:Mg+2HCl=MgCl2+H2↑;
在金属活动顺序中,排在前面的金属可以把排在后面的金属从其盐溶液中置换出来(钾、钙、钠除外),如Fe+CuSO4=Cu+FeSO4;故填:Fe+CuSO4=Cu+FeSO4;
氢气具有还原性,在加热的条件下可将金属氧化物还原为金属单质,如在加热的条件下,氢气将氧化铜还原为金属铜,故填:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
碳具有还原性,在高温的条件下,碳能将金属氧化物还原为金属单质,如在高温的条件下,碳能将氧化铜还原为铜,故填:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

| A. | 硫在氧气中燃烧产生明亮蓝紫色火焰 | |
| B. | 碘酒滴入米汤中,米汤呈蓝色 | |
| C. | 氨气能使湿润的红色石蕊试纸变蓝 | |
| D. | 铁丝在空气中剧烈燃烧,生成黒色固体 |
 如图为A、B两种固体物质的溶解度曲线.请根据图示回答:
如图为A、B两种固体物质的溶解度曲线.请根据图示回答: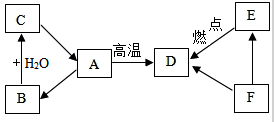 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易于血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:
已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易于血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答: