题目内容
人体内几种液体的正常pH范围如下:
体液 | 血浆 | 胃液 | 胆汁 | 胰液 |
pH | 7.35~7.45 | 0.9~1.5 | 7.1~7.3 | 7.5~8.0 |
下列说法错误的是
A.血浆显碱性 B.胃液和胆汁显酸性
C.胰液比血浆的碱性强 D.胃酸过多的人应少饮碳酸饮料
B 【解析】溶液的pH小于7,溶液呈酸性,pH越小,酸性越强;溶液的pH大于7,溶液呈碱性,pH越大碱性越强;pH等于7,溶液呈中性。由表格中的数据可知,胆汁、血浆、胰液都呈碱性,胃液呈酸性,选B
练习册系列答案
相关题目
兴趣小组同学对“氢氧化钠溶液与稀硫酸混合是否发生了化学反应”进行了如下探究:
【提出问题】氢氧化钠溶液与稀硫酸混合是否发生了化学反应?
【猜想与假设】
a:二者混合发生了化学反应;
b:二者混合没有发生化学反应。
【设计并实验】
实验操作 | 实验现象 | |
甲同学 | 向盛有10mL一定溶质质量分数的氢氧化钠溶液的烧杯中,用胶头滴管慢慢滴入1-2滴稀硫酸,振荡,同时测定溶液的pH | 溶液pH减小但仍大于7 |
乙同学 | 向盛有10mL一定溶质质量分数的氢氧化钠溶液的烧杯中,先滴入几滴无色酚酞试液,然后再加入稀硫酸 | 溶液由红色变为无色 |
【得出结论】氢氧化钠溶液与稀硫酸发生了化学反应。
(1)乙同学认为甲的实验设计不合理,原因是_____________,改进的方法是____________;根据改进后的实验现象说明二者混合后发生了化学反应,写出氢氧化钠溶液与稀硫酸反应的化学方程式__________;甲同学也认为乙的实验设计也不合理,你是否赞同,说出你的理由___________。
【思考与交流】
丙同学在绝热装置中,向分别盛有10mL10%氢氧化钠溶液加入不同体积某浓度的稀硫酸,充分混合后溶液的温度变化曲线如图(混合前稀硫酸和氢氧化钠溶液均为18℃)。
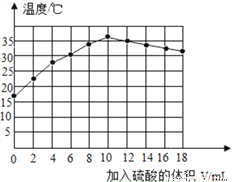
(2)根据图示分析,稀硫酸和氢氧化钠的反应是__________(填吸热、放热)反应,加入稀硫酸_________mL时,二者恰好完全反应.
滴的稀硫酸的量过少 继续滴加稀硫酸使溶液pH等于7或小于7 2NaOH+H2SO4=Na2SO4+H2O 不赞同,因为先滴入几滴酚酞试液时溶液变红色,说明氢氧化钠溶液显碱性,再加入稀硫酸后溶液由红色变成无色,说明此时溶液显中性或酸性,证明此时氢氧化钠和稀硫酸发生了反应 放热 10 【解析】【得出结论】(1)滴加水会使溶液稀释,溶液pH也会减小,但溶液pH减小仍大于7,不能说明氢氧化钠与硫酸反...