题目内容
14. A-F表示初中化学常见的物质,且A、B、C属于不同类别的物质.A和B,B和C都能发生反应,都只能生成两种产物,它们之间转化关系如图所示.
A-F表示初中化学常见的物质,且A、B、C属于不同类别的物质.A和B,B和C都能发生反应,都只能生成两种产物,它们之间转化关系如图所示.(1)若B是世界上年产量最高的金属,D是一种红色的单质,F是一种气体. 请写出反应①的化学方程式为Fe+CuSO4=FeSO4+Cu.
(2)若A是一种气体氧化物,E是大理石的主要成分.写出反应②的化学方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(3)若E在常温下是一种无色液体,A中含有两种元素且A能F发生反应,写出一个符合题意的A与F反应的化学方程式Na2CO3+2HCl=2NaCl+H2O+CO2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑合理均可).
A-F中六种物质属于盐的是D和F(填字母)
分析 (1)根据A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,B是目前世界上年产量最高的金属,所以B是铁,铁和A反应会生成D和E,D是一种红色的单质,所以D是铜,铁和C反应会生成F和E,F是一种气体,所以C可以是硫酸,F就是氢气,E是硫酸亚铁,A就是硫酸铜,然后将推出的各种物质代入转化关系中验证即可;
(2)根据A是一种气体氧化物,A和B反应产生E和D,E是大理石的主要成分,因此A是二氧化碳,B是氢氧化钙,E是碳酸钙,则D是水;A、B、C属于不同类别的物质,且B-氢氧化钙能够和C反应产生碳酸钙沉淀,因此C可以是碳酸钠,则F是氢氧化钠,然后将推出的各种物质代入转化关系中验证即可;
(3)根据A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,A、B、C表示不同类别的化合物,E在常温下是一种无色液体,猜想E是水,酸、碱反应会生成水,二氧化碳和碱反应会生成水和盐,所以猜想B是氢氧化钠,A是盐酸,C是二氧化碳,盐酸和氢氧化钠反应生成氯化钠和水,氢氧化钠和二氧化碳反应生成碳酸钠和水,盐酸和碳酸钠会发生反应,然后将猜想的物质代入转化关系中验证即可.
解答 解:(1)A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,B是目前世界上年产量最高的金属,所以B是铁,铁和Y反应会生成D和E,D是一种红的单质,所以D是铜,铁和C反应会生成F和E,F是一种气体,所以C可以是硫酸,F就是氢气,E是硫酸亚铁,A就是硫酸铜,硫酸铜和铁反应生成硫酸亚铁和铜,铁和硫酸反应生成硫酸亚铁和氢气,推出的各种物质均满足题意,推导合理,所以反应①是铁和硫酸铜反应生成硫酸亚铁和铜,故反应的方程式为Fe+CuSO4=FeSO4+Cu;
(2)A是一种气体氧化物,A和B反应产生E和D,E是大理石的主要成分,因此A是二氧化碳,B是氢氧化钙,E是碳酸钙,则D是水;A、B、C属于不同类别的物质,且B-氢氧化钙能够和C反应产生碳酸钙沉淀,因此C可以是碳酸钠,则F是氢氧化钠,碳酸钠和氢氧化钙反应产生碳酸钙沉淀和氢氧化钠,故反应的方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(3)A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,A、B、C表示不同类别的化合物,E在常温下是一种无色液体,猜想E是水,酸、碱反应会生成水,二氧化碳和碱反应会生成水和盐,所以猜想B是氢氧化钠,A是盐酸,C是二氧化碳,盐酸和氢氧化钠反应生成氯化钠和水,氢氧化钠和二氧化碳反应生成碳酸钠和水,盐酸和碳酸钠会发生反应,猜想的各种物质满足题中的转化关系,猜想正确,所以A与F反应是盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;通过推导可知,A是盐酸,B是氢氧化钠,C是二氧化碳,D是氯化钠,E是水,F是碳酸钠,所以A-F中六种物质属于盐的是:D、F.
故答案为:Na2CO3+2HCl=2NaCl+H2O+CO2↑(或CaCO3+2HCl=CaCl2+H2O+CO2↑合理均可);D和F.
点评 本题为框图式物质推断题,在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系猜想剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可,注意答案的开放性.

 春雨教育同步作文系列答案
春雨教育同步作文系列答案| A. |  铁架台 | B. |  水槽 | C. |  坩锅钳 | D. |  表面皿 |
(1)电石制乙炔气体(C2H2)时产生灰浆和残渣的过程如下:
电石(CaC2)$\underset{\stackrel{\;}{→}}{水}$灰浆$\stackrel{露置于空气}{→}$残渣
其中电石与水反应生成氢氧化钙和乙炔,该反应的化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑.残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:
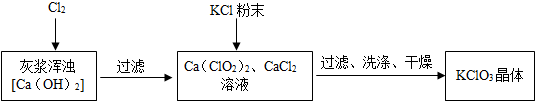
(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)洗涤时,可以选用下列BC作洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
过滤
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl溶液的目的是溶解残渣中的难溶盐):
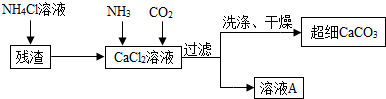
(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
| A. | 火力发电 | B. | 焚烧垃圾 | C. | 建筑粉尘 | D. | 白色污染 |
| A. | H2SO4、KOH、NaCl | B. | KNO3、NaCl、CuSO4 | ||
| C. | AgNO3、NaCl、HCl | D. | H2SO4、Na2SO4、KNO3 |
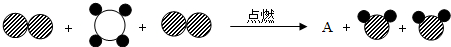
 ”表示碳原子,“
”表示碳原子,“ ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,该生成物A为
”表示氧原子,该生成物A为
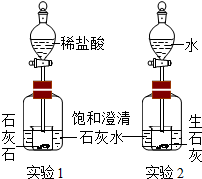 如图,实验一和实验二都会观察到的现象是澄清的石灰水变浑浊.实验一产生这一现象的原因是石灰石和稀盐酸反应生成了二氧化碳,二氧化碳与石灰水中的氢氧化钙反应生成了不溶于水的碳酸钙.实验二产生这一现象的原因是生石灰和水反应放出大量的热使石灰水的温度上升,石灰水中的氢氧化钙的溶解度随着温度的升高而减小,有Ca(OH)2固体析出.
如图,实验一和实验二都会观察到的现象是澄清的石灰水变浑浊.实验一产生这一现象的原因是石灰石和稀盐酸反应生成了二氧化碳,二氧化碳与石灰水中的氢氧化钙反应生成了不溶于水的碳酸钙.实验二产生这一现象的原因是生石灰和水反应放出大量的热使石灰水的温度上升,石灰水中的氢氧化钙的溶解度随着温度的升高而减小,有Ca(OH)2固体析出.