题目内容
某合金由两种元素组成,取该合金8g与足量的稀硫酸充分反应后,如果生成0.2g氢气,该合金中的元素可能是( )
| A、Zn和Fe | B、Cu和Au | C、Zn和Cu | D、Mg和Fe |
分析:根据金属活动性顺序可知,Cu和Au不与稀硫酸反应产生氢气;利用一定质量金属完全反应放出氢气质量=
×金属质量,计算生成0.2g氢气消耗选项所涉及金属铁、锌、镁的质量;然后根据题目的条件:“两种金属混合物8g,与足量稀硫酸反应后生成了0.2g氢气”,推断出两种金属混合物的可能组成.
| 金属的化合价 |
| 金属的相对原子质量 |
解答:解:根据与硫酸反应时铁、锌、镁的化合价都为+2,与足量稀硫酸反应后生成了0.2g氢气,所需要消耗金属的质量分别为:
需要金属铁的质量=0.2g×
=5.6g;
需要金属锌的质量0.2g×
=6.5g;
需要金属镁的质量=0.2g×
=2.4g;Cu和Au不与稀硫酸反应;
根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中“两种金属混合物8g与足量稀硫酸反应后生成了0.2g氢气”,可判断选项混合物中两种金属只可能为金属“铜与锌”的混合物.
故选:C.
需要金属铁的质量=0.2g×
| 56 |
| 2 |
需要金属锌的质量0.2g×
| 65 |
| 2 |
需要金属镁的质量=0.2g×
| 24 |
| 2 |
根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中“两种金属混合物8g与足量稀硫酸反应后生成了0.2g氢气”,可判断选项混合物中两种金属只可能为金属“铜与锌”的混合物.
故选:C.
点评:一定质量金属完全反应放出氢气质量=
×金属质量,利用该公式进行计算时,需要注意到铁在与酸发生置换反应时呈现出+2价.
| 金属的化合价 |
| 金属的相对原子质量 |

练习册系列答案
相关题目
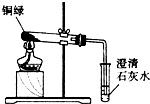
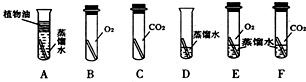
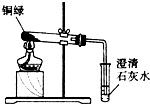
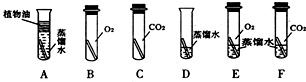
 2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见图1),发表严正声明:中国对其拥有不可置疑的所有权.目前我国正在积极追讨这两件文物.兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿).为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见图1),发表严正声明:中国对其拥有不可置疑的所有权.目前我国正在积极追讨这两件文物.兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿).为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究: ”为铜片):
”为铜片):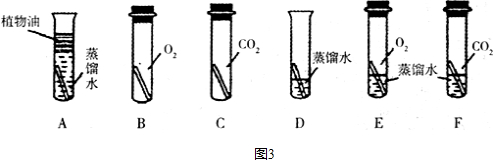
 2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见图1),发表严正声明:中国对其拥有不可置疑的所有权.目前我国正在积极追讨这两件文物.兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿).为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究:
2009年2月12日,我外交部就法国某公司拍卖我国两件重要文物兔首和鼠首(见图1),发表严正声明:中国对其拥有不可置疑的所有权.目前我国正在积极追讨这两件文物.兔首和鼠首均为青铜器(铜、锡合金),表面呈绿色,这是铜器长期暴露在空气中生成了铜锈(铜锈俗称铜绿).为了弄清铜绿的组成和铜生成铜绿的条件,某化学实验小组进行了如下探究: ”为铜片):
”为铜片):