题目内容
12. 钙元素对人类生命和生活具有重要意义.
钙元素对人类生命和生活具有重要意义.(1)在元素周期表中钙元素的信息如图所示.钙原子核内质子数为20.
(2)儿童缺钙可能会导致佝偻病(填“贫血症”或“佝偻病”).
(3)氧化钙能与水反应,此反应可用于ABC.
A.吸收水分 B.制熟石灰 C.加热食物.
(4)熟石灰的化学式为Ca(OH)2,它可用于制备补碘剂Ca(IO3)2,其中碘元素的化合价为+5.
分析 (1)根据元素周期表中的信息来分析;(2)根据钙元素对人体的重要作用来分析解答;(3)根据氧化钙能与水反应的特点分析判断;(4)根据物质的名称写出化学式,根据化合价原则求出元素的化合价.
解答 解:(1)因为原子序数=核电荷数=质子数,元素周期表中左上角的数字表示该元素的核内质子数;故填:20;
(2)人体内的钙元素帮助构成骨骼和牙齿;对凝血、神经及肌肉功能有重要作用,缺钙能导致儿童发育不良或佝偻病;故填:佝偻病;
(3)氧化钙能与水反应生成了熟石灰,此反应放出大量的热,可用于加热食物;故填:ABC;
(4)熟石灰的化学式是:Ca(OH)2,在[Ca(IO3)2]中,由于钙显+2价,氧显-2价,设碘元素的化合价为x,则(+2)+[x+(-2)×3]×2=0 解得x=+5.
故为:Ca(OH)2,+5.
点评 熟悉钙元素的生理作用、氢氧化钙的制取、化合价原则等知识是解答本题的关键.

练习册系列答案
相关题目
20.在稀硫酸中加入一定量的氢氧化钠溶液后,下列实验能证明二者恰好完全中和的是( )
| A. | 滴入适量CuSO4溶液,无蓝色沉淀生成 | |
| B. | 加入适量碳酸钠,无气泡产生 | |
| C. | 滴加紫色石蕊试液,溶液为紫色 | |
| D. | 滴入适量的BaCl2溶液,观察到有白色沉淀 |
4.下列有关化学实验的说法中正确的是( )
| A. | 在铁制品表面刷漆可防止铁生锈,原理是隔绝了铁制品表面的氧气 | |
| B. | 使用pH试纸时,需要先用蒸馏水将其湿润 | |
| C. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢倒入水中,并不断搅拌 | |
| D. | 用红磷和白磷探究燃烧条件的实验结论是燃烧需要可燃物 |
1.用pH试纸测定肥皂水的酸碱度时,如果先将pH试纸用蒸馏水润湿后再把肥皂水滴在试纸上,测得的pH与实际值相比( )
| A. | 偏大 | B. | 偏小 | ||
| C. | 相等 | D. | 可能偏大也可能偏小 |
2.现有X、Y、Z三种金属,只有X与稀硫酸反应,Y与Z的硝酸盐溶液能发生反应,则三种金属活动性顺序由强到弱的是( )
| A. | Z、Y、X | B. | X、Z、Y | C. | X、Y、Z | D. | Z、X、Y |
 市售的碳酸氢钠片是一种白色片状药剂,主要成份为碳酸氢钠(NaHCO3),用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸等有关症状,根据题意,试回答以下问题:
市售的碳酸氢钠片是一种白色片状药剂,主要成份为碳酸氢钠(NaHCO3),用于缓解胃酸过多引起的胃痛、胃灼热感(烧心)、反酸等有关症状,根据题意,试回答以下问题: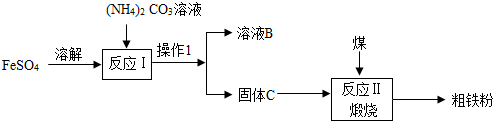

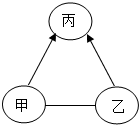 甲、乙、丙是初中化学常见的物质,它们之间有如图所示的相互反应或转化关系.甲、乙、丙分别属于不同类别的化合物,其中丙是氧化物,甲在人体胃液中起帮助消化作用.(图中“-”表示相互反应,“→”表示转化关系;部分反应物、生成物已略去)
甲、乙、丙是初中化学常见的物质,它们之间有如图所示的相互反应或转化关系.甲、乙、丙分别属于不同类别的化合物,其中丙是氧化物,甲在人体胃液中起帮助消化作用.(图中“-”表示相互反应,“→”表示转化关系;部分反应物、生成物已略去)