题目内容
小明知道镁在氧气中燃烧会生成白色的氧化镁固体,但她在空气中点燃镁条时,却发现在白色固体中夹杂着少量淡黄色固体.
<提出问题>为什么会生成黄色固体?
<查阅资料>小明查阅了资料,并记录了下列几种物质的颜色
其他同学认为不必查阅氯化镁的颜色,理由是
<提出猜想>分析资料,小明认为淡黄色固体可能是由镁与空气中的 反应生成的.
<实验探究>小明设计实验证实了自己的猜想,她的方案可能是
<实验结论>小明根据实验结果,写出镁条在空气中燃烧的一个方程式 .
<提出问题>为什么会生成黄色固体?
<查阅资料>小明查阅了资料,并记录了下列几种物质的颜色
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
<提出猜想>分析资料,小明认为淡黄色固体可能是由镁与空气中的
<实验探究>小明设计实验证实了自己的猜想,她的方案可能是
<实验结论>小明根据实验结果,写出镁条在空气中燃烧的一个方程式
考点:实验探究物质的性质或变化规律,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:[查阅资料]根据质量守恒定律确定产物中一定不存在氯化镁;
[提出猜想]根据空气的成分和固体的颜色判断淡黄色固体的来源;
[实验探究]根据在纯氧气中燃烧镁条只生成白色固体,在纯氮气中燃烧镁条只生成淡黄色色固体,可采取在纯纯氮气中燃烧镁条,观察现象的方法;
[实验结论]根据反应的反应物、生成物和反应条件书写方程式.
[提出猜想]根据空气的成分和固体的颜色判断淡黄色固体的来源;
[实验探究]根据在纯氧气中燃烧镁条只生成白色固体,在纯氮气中燃烧镁条只生成淡黄色色固体,可采取在纯纯氮气中燃烧镁条,观察现象的方法;
[实验结论]根据反应的反应物、生成物和反应条件书写方程式.
解答:解:[查阅资料]根据质量守恒定律,化学反应前后元素的种类不变,由于空气中无氯元素,所以燃烧产物中一定不存在氯化镁;
[提出猜想]空气中含有氮气,在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体,而氮化镁为淡黄色,所以淡黄色的固体可能是镁与空气中的氮气反应生成的.
[实验探究]由于在纯氧气中燃烧镁条只生成白色固体氧化镁,在纯氮气中燃烧镁条只生成淡黄色色固体氮化镁,可用在纯氮气中燃烧镁条,观察现象的方法.
[实验结论]镁和氧气在点燃的条件下燃烧生成氧化镁,化学方程式为:2Mg+O2
2MgO;镁和氮气在点燃的条件下反应生成氮化镁,化学方程式:
3Mg+N2
Mg3N2.
故答案为:[查阅资料]空气的成分中不含氯元素;
[提出猜想]氮气(或N2)
[实验探究]将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体
[实验结论]2Mg+O2
2MgO或3Mg+N2
Mg3N2
[提出猜想]空气中含有氮气,在空气中点燃镁条时,生成的白色固体物质中夹杂着少量的淡黄色固体,而氮化镁为淡黄色,所以淡黄色的固体可能是镁与空气中的氮气反应生成的.
[实验探究]由于在纯氧气中燃烧镁条只生成白色固体氧化镁,在纯氮气中燃烧镁条只生成淡黄色色固体氮化镁,可用在纯氮气中燃烧镁条,观察现象的方法.
[实验结论]镁和氧气在点燃的条件下燃烧生成氧化镁,化学方程式为:2Mg+O2
| ||
3Mg+N2
| ||
故答案为:[查阅资料]空气的成分中不含氯元素;
[提出猜想]氮气(或N2)
[实验探究]将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体
[实验结论]2Mg+O2
| ||
| ||
点评:正确理解质量守恒定律的内容,了解燃烧的定义及定义的拓展意义是解决问题的关键,书写化学方程式一定要确定反应物和生成物的化学式,不要忘记配平和条件.

练习册系列答案
相关题目
目前,我国上海、江苏等部分省市发生H7N9禽流感病例,为了防止疫情蔓延,每天用0.2%的过氧乙酸溶液对禽舍进行消毒二次,过氧乙酸的化学式为C2H4O3.则下列有关过氧乙酸的说法正确的是( )
| A、过氧乙酸由三种个元素组成 |
| B、一个过氧乙酸分子中含有二个氢分子 |
| C、过氧乙酸由9个原子构成 |
| D、过氧乙酸中碳元素与氧元素的质量比为1:2 |
据新闻报道,目前中小学生喜欢使用的涂改液中含有许多挥发性的有害物质,长期使用易引起中毒而头晕、头痛,三氯甲烷(CHCl3)就是其中一种.下列关于三氯甲烷组成的叙述中,不正确的是( )
| A、三氯甲烷是有机化合物 |
| B、三氯甲烷是由碳、氢、氯三种元素组成的 |
| C、三氯甲烷的相对分子质量是119.5 |
| D、三氯甲烷是由一个碳原子、一个氢原子和三个氯原子组成的 |
亚硝酸铵(NH4NO2)中有关N的化合价判断正确的是( )
| A、两个N原子均为+1 |
| B、第一个N原子为+3 |
| C、第二个N原子为-5 |
| D、第二个N原子为+3 |
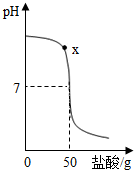 在盛有40g溶质质量分数为20%氢氧化钠溶液的烧杯中,用滴管吸取盐酸逐滴加入盛有氢氧化钠溶液的烧杯中,验证“中和反应会放热”,同时用pH计记录溶液pH的变化,绘制成如图所示的函数图象.
在盛有40g溶质质量分数为20%氢氧化钠溶液的烧杯中,用滴管吸取盐酸逐滴加入盛有氢氧化钠溶液的烧杯中,验证“中和反应会放热”,同时用pH计记录溶液pH的变化,绘制成如图所示的函数图象.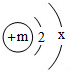 (1)按下列要求选择序号填空.
(1)按下列要求选择序号填空.