题目内容
|
| A. | 氯化铵的溶解度最大 |
|
| B. | 随着温度升高,硫酸钠的溶解度不断增大 |
|
| C. | 40℃时硫酸钠饱和溶液溶质的质量分数为50% |
|
| D. | 把40℃时相同质量的饱和溶液降温到20℃,硫酸钠析出晶体最多 |
| 固体溶解度曲线及其作用.. | |
| 专题: | 结合课本知识的信息;压轴实验题;函数图像的应用. |
| 分析: | 根据固体的溶解度曲线可知:①查出某物质在某温度下的溶解度,从而可以求出同温度下该物质的饱和溶液中溶质的质量分数= |
| 解答: | 解:A、由于固体的溶解度随温度的变化而变化,因此若不说明在哪一温度下,溶解度也就没有意义,故A错误; B、由硫酸钠的溶解度曲线可知,在低于40℃时,硫酸钠的溶解度随温度的升高而增大,高于40℃时,硫酸钠的溶解度随温度的升高而减小,故B错误; C、由于在40℃时,硫酸钠的溶解度是50g,即该温度下,硫酸钠的饱和溶液中溶质的质量分数为 D、由于在低于40℃时,硫酸钠的溶解度随温度的升高而增大,且受温度的影响最大,因此把40℃时饱和溶液降温到20℃,硫酸钠析出晶体最多,故D正确; 故选D |
| 点评: | 本题难度较大,主要考查了固体溶解度曲线所表示的意义,及对固体溶解度概念的理解,从而培养学生的理解能力和应用能力. |

 亮点激活精编提优100分大试卷系列答案
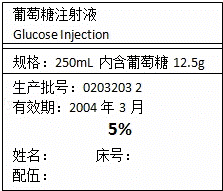
亮点激活精编提优100分大试卷系列答案下列对“化学与生活”的认识,错误的是( )
|
| A. |
| B. |
| C. |
| D. |
|
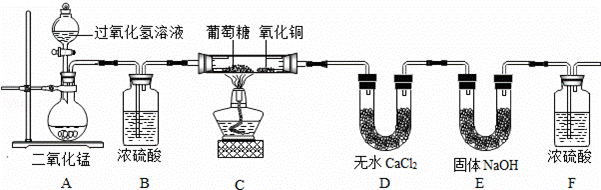
葡萄糖是生命体所需能量的主要来源.
【提出问题】葡萄糖的燃烧产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
【实验设计】为了确定葡萄糖的元素组成,某小组设计了如下实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略).
(1)装置A中发生反应的化学方程式是 .
(2)装置C处氧化铜的作用是 .
【方案评价】
用充有空气的储气球代替装置A,是否更有利于实验的进行? (填“是”或“否”),原因是 .
【数据处理】下表是同学们填写的实验报告,请你帮助完成.
| 实验事实 | 数据分析及结论 |
| 1.8g葡萄糖完全燃烧,得到2.64g CO2和1.08g H2O | 数据分析:
结论:葡萄糖含有C、H、O三种元素 |
如图是某物质的溶解度曲线,60℃时,取100g水配制成该物质的饱和溶液,当温度降低至30℃时所得溶液的质量为( )

|
| A. | 130g | B. | 140g | C. | 160g | D. | 180g |
 ×100%,②比较不同的物质在同一温度下的溶解度的大小,③判断物质的溶解度随温度变化的变化情况,从而比较给等质量的饱和溶液降温时析出晶体的多少等.
×100%,②比较不同的物质在同一温度下的溶解度的大小,③判断物质的溶解度随温度变化的变化情况,从而比较给等质量的饱和溶液降温时析出晶体的多少等.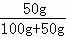 ×100%=33.3%,故C错误;
×100%=33.3%,故C错误;
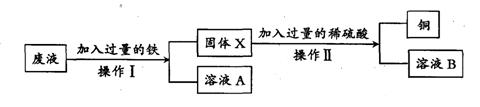
 写出流程图中一种氧化物的名称___________。
写出流程图中一种氧化物的名称___________。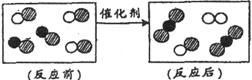 A.反应物和生成物全部是化合物
A.反应物和生成物全部是化合物 3
3