题目内容
15.(1)如图试验中的现象是什么?(2)该反应的实质是什么?(请用符号表示)
(3)小玉在进行上述实验时,滴完酸才想起来其滴加酚酞溶液,滴完后酚酞试液呈现无色.小玉为进一步探究盐酸是否过量,加入硝酸银溶液,产生白色沉淀.据此,小玉认为盐酸过量.小玉的做法对吗?若正确,请写出相关化学方程式;若不正确,请简要说明原因.
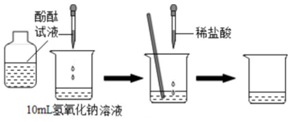
分析 氢氧化钠溶液显碱性,能使酚酞试液变红色,能和稀盐酸反应生成氯化钠和水,反应的实质是氢离子和氢氧根离子结合生成水.
解答 解:(1)如图试验中,滴加酚酞试液时氢氧化钠溶液变红色,滴加足量稀盐酸时,溶液由红色变成无色,因此实验现象是:溶液先变红色,后变成无色.
故答案为:溶液先变红色,后变成无色.
(2)该反应的实质是氢离子和氢氧根离子结合生成水,可以表示为:H++OH-=H2O.
故答案为:H++OH-=H2O.
(3)不正确,这是因为无论稀盐酸是否过量,反应生成的氯化钠能和硝酸银反应生成白色沉淀氯化银和硝酸钠.
故答案为:不正确,这是因为无论稀盐酸是否过量,反应生成的氯化钠能和硝酸银反应生成白色沉淀氯化银和硝酸钠.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.

练习册系列答案
相关题目
20.正确使用和理解化学用语是重要的学科素养,下列说法正确的是( )
| A. | H2O、H2CO3中均含有氢分子 | |
| B. | H2O和H2O2的组成元素相同,但它们的化学性质不同 | |
| C. | Na+、Mg2+、Al3+原子核内质子数均为10 | |
| D. | 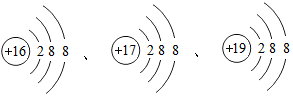 表示的粒子都是阴离子 表示的粒子都是阴离子 |
7.将等质量、等质量分数的氢氧化钠溶液和硫酸溶液混合,混合后的溶液不能与下列物质发生反应的是( )
| A. | Ba(OH)2 | B. | Fe | C. | HCl | D. | FeCl2 |
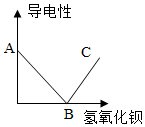 溶液具有导电性是因为溶液中存在着自由移动的离子,当接通电路时,这些自由移动的离子能定向移动,产生电流,而且在一定条件下,离子浓度越高,导电性就越强.某同学做了如下的实验:向硫酸溶液中逐渐滴加氢氧化钡溶液,并利用相应的仪器测定溶液的导电性,绘制如下的图.请回答下列的问题.
溶液具有导电性是因为溶液中存在着自由移动的离子,当接通电路时,这些自由移动的离子能定向移动,产生电流,而且在一定条件下,离子浓度越高,导电性就越强.某同学做了如下的实验:向硫酸溶液中逐渐滴加氢氧化钡溶液,并利用相应的仪器测定溶液的导电性,绘制如下的图.请回答下列的问题.