题目内容
14.等质量的锌、铁分别与足量的稀硫酸完全反应,产生氢气的质量m与反应时间t的关系如图所示.其中合理的是( )| A. | 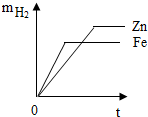 | B. | 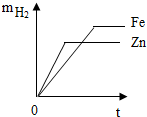 | C. | 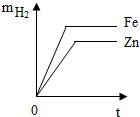 | D. | 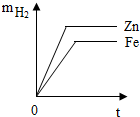 |
分析 根据等质量的两种金属与酸完全反应放出氢气质量的大小,利用化学方程式的计算,可以判断关系图中两条线与金属的对应关系.金属活动性越强,金属与酸反应越剧烈,在相同时间则放出氢气的量越多,即反应速率越快.
解答 解:等质量的铁、锌与足量的稀硫酸完全反应时,铁产生的氢气比锌产生的氢气多,所以铁的曲线在上边,因为锌比铁活泼,所以锌反应的快,最先到达最高点.
故选B.
点评 等质量的铁、锌与酸完全反应放出氢气的质量由大到小的关系为:铁>锌.

练习册系列答案
相关题目
20.金属钠在空气中燃烧,可以生成淡黄色固体过氧化钠(Na2O2),Na2O2中氧元素的化合价为( )
| A. | -1 | B. | -2 | C. | +1 | D. | +2 |
1.下列有关物质燃烧现象的叙述中,正确的是( )
| A. | 铁丝在氧气中燃烧:火星四射,生成红色固体 | |
| B. | 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体 | |
| C. | 镁条在氧气中燃烧:发出耀眼的白光,生成白色的氧化镁固体 | |
| D. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 |
19.如表是KNO3和NaNO3在不同温度时的溶解度(单位:g).
(1)从表中数据看出,KNO3与NaNO3溶解度受温度影响更大的是KNO3.
(2)10℃时,100g水中最多溶解NaNO380g.
(3)60℃时,向盛100g水的烧杯中加入100gKNO3,配成溶液,然后降温至20℃,烧杯中析出的晶体为68.4g.(精确到0.1)
(4)KNO3和NaNO3在t℃时的溶解度均为Wg,分析上表数据可推知,W的数值所在的最精确范围是125~136.
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaNO3 | 80 | 87 | 95 | 103 | 114 | 125 | 136 | 150 | 163 | 170 |
(2)10℃时,100g水中最多溶解NaNO380g.
(3)60℃时,向盛100g水的烧杯中加入100gKNO3,配成溶液,然后降温至20℃,烧杯中析出的晶体为68.4g.(精确到0.1)
(4)KNO3和NaNO3在t℃时的溶解度均为Wg,分析上表数据可推知,W的数值所在的最精确范围是125~136.
3.下列气体中约占空气总体积21%的是( )
| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
4.一种硫元素的氧化物中,硫元素和氧元素的质量比为2:3,则此硫原子和氧原子的个数比( )
| A. | 1:1 | B. | 1:3 | C. | 1:2 | D. | 3:1 |
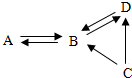 A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去):
A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去):