题目内容
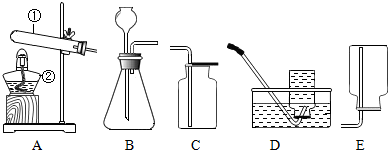
9.实验室常用如图2所示装置制取气体,请你根据所学知识回答下列问题.
(1)写出图中标有①、②的仪器名称酒精灯、量筒.
(2)甲同学用A和C装置可制取氧气,请写出加热高锰酸钾制氧气的文字表达式高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.他在该装置试管内的导管口处添加了一团棉花,其目的是:防止加热时高锰酸钾小颗粒进入导气管.
(3)乙同学选用B和D两种装置,则他是否能制取并测量氧气的体积?是(填“是”或“否”).
(4)丙同学用分解过氧化氢溶液的方法制取并收集氧气;该方法有许多优点,如:①②(填序号);
①产物无污染 ②不需加热 ③需加热 ④生成物只有氧气
(5)丁同学对甲同学的装置产生了质疑.他认为加热高锰酸钾时,在试管较小的空间内氧气浓度高,温度也较高,而棉花是易燃物质,实验时可能会发生危险,他建议采用不易燃烧的丝状物质代替棉花更安全.丁同学的观点是否正确,你认为最科学的判断依据是③(填序号).
①依据教科书的观点 ②依据老师的观点 ③依据实验事实
(6)若用图2装置进行“排空气法”收集制取的氧气,请把图中的“导气管”补画完整.
分析 (1)根据实验室常用仪器的名称与用途,进行解答;
(2)根据高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,写出反应的文字表达式;根据高锰酸钾制取氧气装置的注意事项分析棉花的作用即可;
(3)制取氧气为固体和液体的反应,无需加热,所以B装置可以.量取气体的体积的常用方法是排水法,根据水的体积和气体的体积相等,则用量筒量取的水的体积就是气体的体积;
(4)根据用分解过氧化氢溶液的方法制取氧气的特点分析;
(5)根据实践是检验真理的唯一标准观点回答;
(6)根据氧气的密度与空气的密度的关系分析装置的特点.
解答 解:(1)图中标号的仪器名称:①是酒精灯;②是量筒;
(2)高锰酸钾在加热条件下生成锰酸钾、二氧化锰和氧气,反应的文字表达式:高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;实验时应在试管口放一团棉花,其作用是:防止高锰酸钾颗粒进入导气管;
(3)B和D装置相连.B装置中,试管中加过氧化氢和二氧化锰就可以制的氧气,而D装置中集气瓶中装满水,则制得的氧气进入集气瓶,气体压力将水压入量筒,则气体的体积就是量筒中的水的体积,所以这个装置既可以制得氧气又可以测量氧气的体积;
(4)用分解过氧化氢溶液与二氧化锰的方法制取氧气与用加热的方法制取氧气相比,不需要加热,副产物是水,无污染,故选择①②;
(5)实践是检验真理的唯一标准,判断一种观点是否正确,要依据实验事实,因此选择③;
(6)由于氧气的密度比空气大,可用向上排空气法收集,也就是从长导管进入,将空气挤压到集气瓶上部,通过短导管排出;装置如下: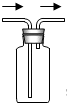
故答案为:(1)酒精灯;量筒;(2)高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气;防止加热时高锰酸钾小颗粒进入导气管;(3)是;(4)①②;(5)③;
(6) .
.
点评 本考点主要考查气体的制取装置和收集装置的选择,同时也考查了文字表达式的书写和仪器的名称,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.

 阅读快车系列答案
阅读快车系列答案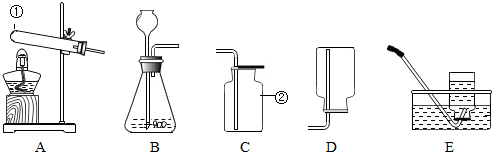
(1)写出指定仪器的名称:①试管 ②集气瓶
(2)实验室用高锰酸钾制取氧气时,在试管口要放一团棉花,原因是为了防止高锰酸钾粉末进入导管,可选用的发生装置是A(填编号),收集装置可选择E,理由是氧气不易溶于水,该反应的文字表达式是高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气.
(3)如果用排空气法收集氧气,验满的方法是将带火星的木条平放在集气瓶口,木条复燃,证明氧气满了.
(4)检查B装置气密性时,用止水夹夹紧橡皮管,从长颈漏斗中倒入水至淹没下端管口,使长颈漏斗中形成一段水柱,过一会儿,水柱不下降证明气密性良好.
(5)查阅资料回答问题:
| 物质 | 制取气体的药品 | 反应条件 | 气体的物理性质 |
| 氯气 | 二氧化锰固体和浓盐酸 | 加热 | 可溶于水,密度比空气大 |
②制取氯气不可以(填“可以”或“不可以”)采用装置B,理由是二氧化锰固体和浓盐酸制氯气需要加热.
| A. | 固态物质受热后变为气态物质,不一定是物理变化 | |
| B. | 生活中的爆炸不一定是化学变化 | |
| C. | 液态物质变为气态物质不一定是化学变化 | |
| D. | 变化前后的物质种类不同,不一定是化学变化 |
| A. | 硫酸镁 | B. | 氯化钾 | C. | 磷酸钙 | D. | 碳酸氢铵 |