题目内容
16.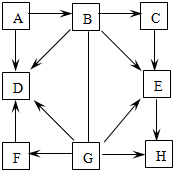 如图中的A~H表示几种初中化学常见的含有氧元素的化合物,其中A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素;E、H属于氧化物;B俗称苏打,F与石灰乳可制农药波尔多液.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
如图中的A~H表示几种初中化学常见的含有氧元素的化合物,其中A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素;E、H属于氧化物;B俗称苏打,F与石灰乳可制农药波尔多液.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.(1)F是由离子(选填“分子”、“原子”或“离子”)构成的.
(2)H的名称是水.
(3)写出C→E反应的化学方程式CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
(4)写出F→D反应的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
分析 根据A~H表示几种初中化学常见的含有氧元素的化合物,B俗称苏打,所以B是碳酸钠,F与石灰乳可制农药波尔多液,所以F是硫酸铜,A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素,E、H属于氧化物,A会转化成B、D,B会转化成D,所以A是氢氧化钠,D是硫酸钠,G会转化成硫酸铜、硫酸钠,所以G是硫酸,E是含碳氧化物,所以E是二氧化碳,C是碳酸钙,H是水,然后将推出的物质进行验证即可.
解答 解:(1)A~H表示几种初中化学常见的含有氧元素的化合物,B俗称苏打,所以B是碳酸钠,F与石灰乳可制农药波尔多液,所以F是硫酸铜,A、B、D均含钠元素,B、C、E均含碳元素,D、F、G均含硫元素,E、H属于氧化物,A会转化成B、D,B会转化成D,所以A是氢氧化钠,D是硫酸钠,G会转化成硫酸铜、硫酸钠,所以G是硫酸,E是含碳氧化物,所以E是二氧化碳,C是碳酸钙,H是水,经过验证,推导正确,所以F是由离子构成的;
(2)通过推导可知,H的名称是水;
(3)C→E的反应是碳酸钙在高温的条件下生成氧化钙和二氧化碳,化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(4)F→D的反应是氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
故答案为:(1)离子;
(2)水;
(3)CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;
(4)CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 精英口算卡系列答案
精英口算卡系列答案(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比实验:
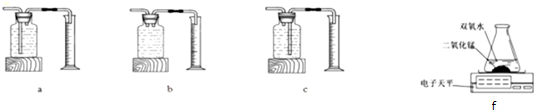
Ⅰ.将4.0gKClO3与0.5gMnO2均匀混合加热
Ⅱ.将4.0gKClO3与xgCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑,Ⅱ中x的值应为0.5.
(2)乙探究了影响过氧化氢分解速度的某种因素.实验数据记录如下:
| 过氧化氢溶液的质量 | 过氧化氢的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
实验结论:在相同条件下,过氧化氢溶液的浓度越大,过氧化氢分解得越快.
丙用如图f装置进行实验,通过比较相同时间装置所减少的质量也能达到实验目的.
(3)还有哪些因素能影响过氧化氢溶液的分解速率?设计实验验证.
| A. | 生石灰和氯化钠 | B. | 硫酸钡和硝酸钾 | C. | 硫酸钡和碳酸钡 | D. | 氯化钠和硝酸铵 |
| A. | 大理石 | B. | 钛合金 | C. | 液氧 | D. | 矿泉水 |
| A. | 原子核 | B. | 电子 | C. | 质子 | D. | 中子 |
| A. | 用水来灭火,是因为降低了可燃物的着火点 | |
| B. | 油锅着火时可用锅盖盖灭,是因为隔绝了空气 | |
| C. | 木炭在氧气中燃烧比在空气中燃烧更剧烈,是因为氧气浓度不同 | |
| D. | 山林中开辟的隔离带可以控制火势蔓延,是因为隔离了可燃物 |
| A. | +2 | B. | +3 | C. | +4 | D. | +6 |
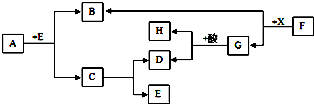 如图表示某些物质间的转化关系(反应条件均略去),其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属,B、D、E均为无色气体.请回答:
如图表示某些物质间的转化关系(反应条件均略去),其中A为天然气的主要成分,C为相对分子质量最小的氧化物,F为红棕色粉末,G为最常见的金属,B、D、E均为无色气体.请回答: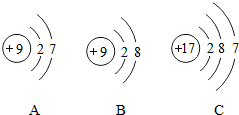 如图是A,B,C三种粒子的结构示意图.
如图是A,B,C三种粒子的结构示意图.