题目内容
18.现将混有少量O2和CO2的N2通过以下几个装置,最后得到干燥的纯净的氮气,请回答: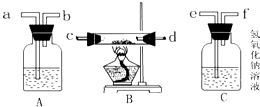
(1)各装置的接口顺序为:
混合气→e、f接a、b接c
(2)B装置中大玻璃管内的固体物质是铜粉
(3)A装置中的液体物质是浓硫酸,A装置的作用是吸水干燥
(4)C装置发生的反应方程式为CO2+2NaOH=Na2CO3+H2O.
分析 混有少量O2和CO2的N2,最后得到干燥的纯净的氮气,需要通过氢氧化钠溶液除去二氧化碳,通过铜粉除去氧气,通过浓硫酸除去水蒸气得到氮气,除杂应该先除去二氧化碳,再除去水蒸气,最后通过灼热的铜粉,防止潮湿的气体可能会导致试管炸裂,据此分析.
解答 解:混有少量O2和CO2的N2,最后得到干燥的纯净的氮气,需要通过氢氧化钠溶液除去二氧化碳,通过铜粉除去氧气,通过浓硫酸除去水蒸气得到氮气,因此显通过氢氧化钠溶液除去二氧化碳,然后通过浓硫酸干燥,否则不能除去水蒸气;最后通过灼热的铜粉,除去氧气,防止含有水分的氧气进入玻璃管引起炸裂,因此装置的顺序为CAB;进气管都是长管,目的是使气体能够和试剂充分接触,达到除杂、干燥的目的;因此:
(1)各装置的接口顺序为:混合气→e→f→a→b→c;故填:e、f、a、b、c;
(2)B装置的目的是除去氧气,因此大玻璃管内的固体物质是铜粉;故填:铜粉;
(3)A装置的目的是吸水干燥,因此是浓硫酸;故填:浓硫酸;吸水干燥;
(4)C装置是二氧化碳和氢氧化钠反应产生碳酸钠和水,故反应的方程式为:CO2+2NaOH=Na2CO3+H2O.
点评 本题考查了气体的除杂、干燥等,分析时注意除杂的试剂及操作的顺序、操作的原理等是解题的关键.

练习册系列答案
相关题目
9.下列有关说法正确的是( )
| A. | 金属资源中金、银、铜、铁等在地壳中主要以单质的形式存在 | |
| B. | 炼铁时将铁矿石、焦炭等原料放入高炉,最后从出铁口得到纯铁 | |
| C. | 地壳中含量最多的金属元素是铁元素 | |
| D. | 金属资源有限,不能随意开采 |
13.下列物质属于单质的是( )
| A. | 二氧化碳 | B. | 液氧 | C. | 冰水混合物 | D. | 河水 |
10.下列物质属于溶液的是( )
| A. | 牛奶 | B. | 硫酸 | ||
| C. | 酒精 | D. | 碘溶解在汽油里面 |
8.做馒头时在发酵的面团中加入某种物质,既能除去面团中的酸又能使馒头变软,则加入的这种物质为( )
| A. | 氢氧化钠 | B. | 碳酸钠 | C. | 氧化钙 | D. | 氯化钠 |