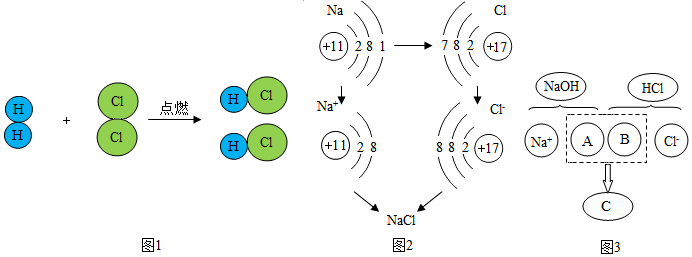
题目内容
4.下图是某兴趣小组设计的四个实验装置,其中实验目的能够达到的是( )| A. |  探究分子的运动 | B. |  探究燃烧的三个条件 | ||
| C. |  测定空气中氧气的含量 | D. |  验证质量守恒定律 |
分析 氨水显碱性,能使酚酞试液变红色;
可燃物燃烧的条件是:与氧气接触,温度达到可燃物的着火点,二者必须同时具备,缺一不可;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳.
解答 解:A、实验过程中,B中的酚酞试液不变色,说明空气中的物质不能使酚酞试液变红色,A中的酚酞试液变红色,通过对比可知,A中的酚酞试液变红色是因为C中的浓氨水导致的,进一步说明浓氨水中的氨分子是不断运动的,当运动到A中时,和水结合成氨水,从而使酚酞试液变红色,该选项能够达到实验目的;
B、实验过程中,白磷燃烧,红磷不能燃烧,说明燃烧需要温度达到可燃物的着火点,而无法检验燃烧是否需要氧气,该选项不能达到实验目的;
C、实验过程中,气球会膨胀、收缩,降至室温时,气球变瘪,无法判断空气中氧气的含量,该选项不能达到实验目的;
D、实验过程中,碳酸钠和稀盐酸反应生成的二氧化碳逸出,无法验证质量守恒定律,该选项不能达到实验目的.
故选:A.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
15.下列物质的用途中,利用其物理性质的是( )
| A. | 氧气用于炼钢 | B. | 氢气作燃料 | ||
| C. | 氧化钙用作干燥剂 | D. | 干冰用于人工降雨 |
19.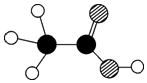 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 表示一个碳原子,
表示一个碳原子, 表示一个氢原子,
表示一个氢原子, 表示一个氧原子,下列说法不正确的是( )
表示一个氧原子,下列说法不正确的是( )
 食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中
食醋是厨房中常用的调味品,它的主要成分是乙酸,乙酸分子的模型如图所示,其中 表示一个碳原子,
表示一个碳原子, 表示一个氢原子,
表示一个氢原子, 表示一个氧原子,下列说法不正确的是( )
表示一个氧原子,下列说法不正确的是( )| A. | 乙酸的化学式为C2H4O2 | |
| B. | 乙酸的相对分子质量为60 | |
| C. | 乙酸中碳元素的质量为60% | |
| D. | 乙酸中碳原子、氢原子、氧原子的原子个数比为1:2:1 |
16.下表为氯化铵和氯化钠在不同温度下的溶解度:
下列说法正确的是( )
| 温度/oC | 0 | 10 | 20 | 30 | 40 | 50 |
| NH4Cl溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 |
| NaCl溶解度/g | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 |
| A. | 20℃时,氯化钠的饱和溶液中溶质质量分数为36% | |
| B. | 由表中数据可知,氯化钠的溶解度受温度影响更大 | |
| C. | 将50℃NH4Cl的饱和溶液降温到20℃,析出13.2克NH4Cl | |
| D. | 氯化铵与氯化钠溶解度相等的温度在10℃-20℃之间 |
13. X、Y两种固体物质的溶解度曲线如图所示.有关叙述正确的是( )
X、Y两种固体物质的溶解度曲线如图所示.有关叙述正确的是( )
 X、Y两种固体物质的溶解度曲线如图所示.有关叙述正确的是( )
X、Y两种固体物质的溶解度曲线如图所示.有关叙述正确的是( )| A. | X比Y的溶解度大 | |
| B. | t2℃时,X和Y的饱和溶液降到t1℃,析出的X一定比Y多 | |
| C. | 向M点的130gX溶液中加入30gX固体能得到t2℃X的饱和溶液 | |
| D. | t1℃时,X和Y的饱和溶液升温到t2℃,溶质的质量分数都增大 |
5.2015年10月,中国女科学家屠呦呦因发现了青蒿素(C11H22O7)而获得诺贝尔生理学或医学奖.下列有关青蒿素的说法错误的是( )
| A. | 一个青蒿素分子共有40原子构成 | |
| B. | 青蒿素由碳、氢、氧三种元素组成 | |
| C. | 青蒿素中碳、氢、氧元素的质量比为14:22:5 | |
| D. | 青蒿素中氢元素的质量分数最小 |

 液氢和液氧是火箭发射的常用推进剂.已知卫星要被送达预定轨道,火箭至少要充分燃烧200kg 的液氢才能产生足够能量.请依据相关反应的化学方程式计算:为满足这些液氢完全燃烧,至少应在火箭发动机中装入多少千克的液氧?
液氢和液氧是火箭发射的常用推进剂.已知卫星要被送达预定轨道,火箭至少要充分燃烧200kg 的液氢才能产生足够能量.请依据相关反应的化学方程式计算:为满足这些液氢完全燃烧,至少应在火箭发动机中装入多少千克的液氧?