题目内容
18.硫酸亚铁(FeSO4)可用于治疗缺铁性贫血,某贫血患者每天需补充1.40g铁元素,服用的药物中含硫酸亚铁的质量至少为多少?分析 此题需要先计算硫酸亚铁的含铁质量分数,然后利用铁的质量除以铁的质量分数即可求出硫酸亚铁的质量.
解答 解:先计算硫酸亚铁中铁的质量分数,然后用铁的质量除以其质量分数即可.
硫酸亚铁FeSO4的相对分子质量=56+32+16×4=152,
FeSO4的Fe的质量分数为:$\frac{56}{152}×100%$=$\frac{7}{19}×100%$,
则FeSO4的质量为:1.40g÷($\frac{7}{19}×100%$)=3.80g
答:服用的药物中含硫酸亚铁的质量至少为3.80g.
点评 此题是对化学式计算的考查,主要利用了元素的质量等于物质的质量乘以元素的质量分数的计算方法,属基础性化学计算题.

练习册系列答案
相关题目
6.某无色气体,密度约为空气密度的$\frac{2}{9}$,且极难溶于水,那么收集可用的方法( )
①向上排空气法 ②向下排空气法 ③排水法.
①向上排空气法 ②向下排空气法 ③排水法.
| A. | ②或③ | B. | ①或③ | C. | ①②③均可 | D. | 无法确定 |
13.氧化汞受热分解微观示意图如图所示,据图得出的下列结论中错误的是( )
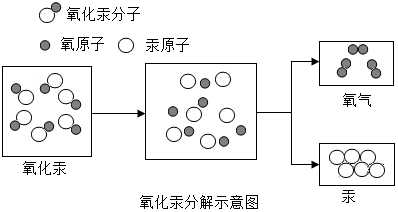

| A. | 氧化汞受热时分解为汞和氧气 | |
| B. | 在化学变化中分子可以再分,而原子不能再分 | |
| C. | 所有的物质都是由分子构成的 | |
| D. | 保持汞的化学性质的最小粒子是汞原子,保持氧化汞的化学性质的最小粒子是氧化汞分子 |
3.盛有饱和石灰水溶液的烧杯敞口放置在空气中,较长时间后,石灰水表面形成了一层“白 膜”(假设水没有减少).下列说法正确的是( )
| A. | “白膜”为反应生成的碳酸钙固体 | B. | 此时该溶液仍为饱和溶液 | ||
| C. | 因析出氢氧化钙固体而形成“白膜” | D. | 给饱和石灰水降温,溶液会变浑浊 |
7.下列有关说法或做法错误的是( )
| A. | 冰水共存物属于纯净物 | |
| B. | 水电解时所生成氢气和氧气的质量比为2:1 | |
| C. | 点燃氢气之前先检验其纯度 | |
| D. | 水沸腾时可冲起壶盖,说明温度升高分子间隔会增大 |
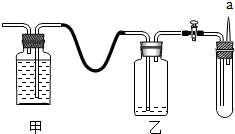 某小组利用右图装置完成O2、CH4、CO或CO2的有关实验.实验过程中,他们通过向甲中充入空气,匀速将乙中的气体(该气体为上述气体中的某一种)排入试管中.
某小组利用右图装置完成O2、CH4、CO或CO2的有关实验.实验过程中,他们通过向甲中充入空气,匀速将乙中的气体(该气体为上述气体中的某一种)排入试管中.