题目内容
9.表面有铁锈(主要成分是Fe2O3)的铁片与稀硫酸反应的化学方程式为Fe2O3+3H2SO4=Fe2 (SO4) 3+3H2O和Fe+H2SO4=FeSO4+H2↑.铜和稀硫酸不反应,与浓硫酸在一定条件下反应的化学方程式为:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+X↑+2H2O,则X的化学式为SO2(填化学式).分析 酸的化学性质主要包括以下几点:能使指示剂变色、能与活泼金属反应、能与金属氧化物反应、能与碱反应、能与某些盐反应;化学方程式的书写主要做好以下几个方面:反应物、生成物、反应条件、化学式的书写、配平、沉淀气体的标注等.化学反应都遵循质量守恒定律.
解答 解:带有铁锈的铁片含有两种物质:铁锈(主要成分是Fe2O3)属于金属氧化物与酸反应生成盐和水、铁属于活泼金属与酸发生置换反应生成盐和氢气;铜属于不活泼金属与稀酸不反应,但与浓硫酸反应;根据质量守恒定律反应前后原子的种类、个数都不变.
故答案为:Fe2O3+3H2SO4=Fe2 (SO4) 3+3H2O;Fe+H2SO4=FeSO4+H2↑;SO2
点评 此题重点考查了酸的化学性质、有关化学方程式的书写和质量守恒定律的内容.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
19.下列各组物质中,富含蛋白质的是( )
| A. | 牛油、奶油 | B. | 米饭、土豆 | C. | 香蕉、桃子 | D. | 鸡蛋、牛奶 |
17.每年的6月5日为世界环境日,它的确立反映了世界各国人民对环境问题的认识和态度,表达了人类对美好环境的向往和追求,2015年我国确立的环境日主题是“践行绿色生活”,下列做法不符合这一主题的是( )
| A. | 购物尽量用塑料袋,少用布袋 | B. | 使用节能灯泡,做到人走灯灭 | ||
| C. | 少开私家车,多乘公交车 | D. | 节约用水,关紧水龙头 |
19.金属材料有着广泛的用途.
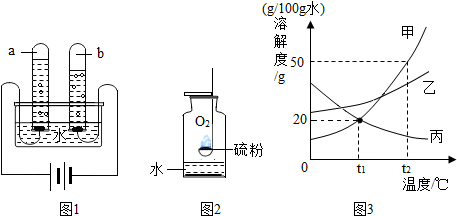
(1)图1所示用品中,利用金属导电性的是B(填字母序号).
(2)下表是一些金属的熔点数据.

铅锡合金中某种金属的质量分数与合金的熔点有如图2所示的关系,其中横坐标表示的是Sn(填化学式)的质量分数;当合金熔点最低时,合金中铅与锡的质量比为2:3.
(3)新型材料纳米级Fe粉在空气中易自燃,能用作高效催化剂,实验室采用还原法制备纳米级Fe粉,流程如图3:
①铁丝在空气中只能灼成红热、离火变冷,而纳米级Fe粉在空气中易自燃,说明物质燃烧的剧烈程度与药品的状态(可燃物与氧气的接触面积)有关.
②写出Ⅱ中用氢气从FeCl2置换出铁的反应方程式H2+FeCl2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl.
在Ⅱ中通入氮气的目的是排尽空气,防止生成的铁粉被反应.
(4)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较强的金属首先被腐蚀.造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是D.(填编号)
A、银块 B、铜块 C、锡块 D、锌块
(5)用下列试剂探究不同金属与酸反应的速率不同:锌片、铁片、5%盐酸.取质量相等的上述两种金属(表面积相同),分别放入溶质质量分数5%的足量稀盐酸中.
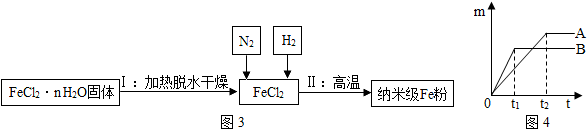
①线B对应的金属是Zn.
②线A对应的金属与稀盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑.
(6)某兴趣小组的同学将一块不纯的铁片5.6g投入到足量的稀盐酸中,充分反应后生成了0.2g气体,则该铁片中混有的杂质一定不可能是D.
A、铝和锌 B、镁和锌 C、镁和铜 D、锌和铜.
(1)图1所示用品中,利用金属导电性的是B(填字母序号).
(2)下表是一些金属的熔点数据.

| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
(3)新型材料纳米级Fe粉在空气中易自燃,能用作高效催化剂,实验室采用还原法制备纳米级Fe粉,流程如图3:
①铁丝在空气中只能灼成红热、离火变冷,而纳米级Fe粉在空气中易自燃,说明物质燃烧的剧烈程度与药品的状态(可燃物与氧气的接触面积)有关.
②写出Ⅱ中用氢气从FeCl2置换出铁的反应方程式H2+FeCl2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl.
在Ⅱ中通入氮气的目的是排尽空气,防止生成的铁粉被反应.
(4)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较强的金属首先被腐蚀.造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是D.(填编号)
A、银块 B、铜块 C、锡块 D、锌块
(5)用下列试剂探究不同金属与酸反应的速率不同:锌片、铁片、5%盐酸.取质量相等的上述两种金属(表面积相同),分别放入溶质质量分数5%的足量稀盐酸中.

①线B对应的金属是Zn.
②线A对应的金属与稀盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑.
(6)某兴趣小组的同学将一块不纯的铁片5.6g投入到足量的稀盐酸中,充分反应后生成了0.2g气体,则该铁片中混有的杂质一定不可能是D.
A、铝和锌 B、镁和锌 C、镁和铜 D、锌和铜.