题目内容
19.最适合将粉末状固体装入干净试管的方法是( )| A. | 用纸槽盛装,然后送至试管底部,缓缓竖起 | |
| B. | 直接用试管口插入试剂瓶取用粉末 | |
| C. | 用药匙向试管中加入固体 | |
| D. | 拿试剂瓶直接往试管中倾倒粉末 |
分析 根据取用粉末状固体药品使用纸槽或药匙,用纸槽将粉末状固体送入试管后直立起试管解答.
解答 解:
A、取用粉末状固体药品使用纸槽或药匙,用纸槽将粉末状固体送入试管后直立起试管,故正确;
B、直接用试管口插入试剂瓶取用粉末,药品会粘在试管壁上,污染试剂,故错误;
C、用药匙向试管中加入固体,药品会粘在试管壁上,故错误;
D、拿试剂瓶直接往试管中倾倒粉末,药品会粘在试管壁上,故错误;
答案:A
点评 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
10.由(NH4)2S、(NH4)2SO4、(NH4)2HPO4组成的混合物中,已知氮元素的质量分数为28%,则混合物中氧元素的质量分数为( )
| A. | 32% | B. | 68% | C. | 28% | D. | 8% |
7.用一氧化碳还原6.0g氧化铁,最终得到剩余物5.8g,剩余物的成分不可能是( )
| A. | Fe和Fe2O3 | B. | Fe2O3和FeO | C. | Fe和FeO | D. | Fe3O4 |
14.下列各组物质的溶液,只需组内物质相互反应就能区别的是( )
| A. | Ba(OH)2、Na2SO4、MgCl2、HCl | B. | BaCl2、K2SO4、Na2CO3、KOH | ||
| C. | FeCl3、HNO3、NaCl、NaOH | D. | H2SO4、KCl、ZnCl2、CuCl2 |
4.天文学家观察到“百武”彗星因受到越来越强的阳光照射而产生喷气现象.喷出气体包括:CO、CH3OH(甲醇)、HCHO(甲醛)、HCN(氢氰酸)等有毒物质和水蒸气.根据这一信息可以推测( )
| A. | “百武”彗星至少含有C、H、N、O元素 | |
| B. | “百武”彗星中存在单质和化合物 | |
| C. | “百武”彗星喷出气体至少含有2种氧化物 | |
| D. | “百武”彗星可能存在生命 |
9.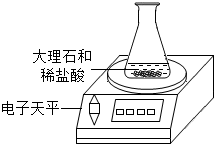 为了探究影响化学反应速率的因素,某学习小组同学选取成分完全相同的大理石碎屑、块状大理石两种样品各15克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图.每隔2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前20分钟数据如下表.(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑)
为了探究影响化学反应速率的因素,某学习小组同学选取成分完全相同的大理石碎屑、块状大理石两种样品各15克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图.每隔2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前20分钟数据如下表.(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑)
(1)CaCO3中碳元素的质量分数是12%.
(2)实验过程中,通过观察如图装置中的电子天平读数不再变化现象可判断反应结束.
(3)结合表格分析,块状大理石与稀盐酸反应最终能生成5.5克二氧化碳.
(4)当反应进行到20分钟时,块状大理石中有多少克碳酸钙与稀盐酸发生了反应?(要求写出计算过程)
 为了探究影响化学反应速率的因素,某学习小组同学选取成分完全相同的大理石碎屑、块状大理石两种样品各15克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图.每隔2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前20分钟数据如下表.(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑)
为了探究影响化学反应速率的因素,某学习小组同学选取成分完全相同的大理石碎屑、块状大理石两种样品各15克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图.每隔2分钟读取一次电子天平的示数,据此计算生成的二氧化碳的质量,并记录前20分钟数据如下表.(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑)(1)CaCO3中碳元素的质量分数是12%.
(2)实验过程中,通过观察如图装置中的电子天平读数不再变化现象可判断反应结束.
(3)结合表格分析,块状大理石与稀盐酸反应最终能生成5.5克二氧化碳.
| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 大理石碎屑生成的CO2质量/克 | 0 | 1.8 | 2.8 | 3.4 | 3.9 | 4.3 | 4.8 | 5.2 | 5.5 | 5.5 | 5.5 |
| 块状大理石生成的CO2质量/克 | 0 | 0.6 | 1.2 | 1.7 | 2.2 | 2.7 | 3.2 | 3.6 | 3.9 | 4.2 | 4.4 |
 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.