题目内容
8.葡萄糖(C6H12O6)、乙酸(CH3COOH)和尿素[CO(NH2)2]组成的混合物240g,在一定条件下完全燃烧,生成水的质量是( )| A. | 48g | B. | 72g | C. | 120g | D. | 144g |
分析 葡萄糖C6H12O6中H元素质量分数=$\frac{1×12}{180}×100%$≈6.67%
乙酸CH3COOH中氢元素质量分数=$\frac{1×4}{60}×100%$≈6.67%
尿素CO(NH2)2中H元素质量分数=$\frac{1×4}{60}×100%$≈6.67%
所以,混合物中H元素质量分数为6.67%,据此计算混合物中H元素质量,最后利用水中氢元素的质量分数,计算生成水的质量
解答 解:葡萄糖C6H12O6、乙酸CH3COOH、尿素CO(NH2)2三种物质中H元素质量分数相等,均约为6.67%,故混合物中H元素的质量分数为6.67%,
三种物质完全燃烧生成水的质量=$\frac{240g×6.67%}{\frac{1×2}{18}×100%}$=144g;
故选D.
点评 发现三种物质中H元素质量分数相等是解决本问题的技巧与关键,此类问题中元素的质量分数往往有一定的特殊关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.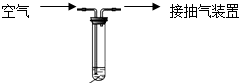 二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
为测定某地空气中二氧化硫的含量,某中学环保小组按上图所示的实验装置进行如下实验:向试管中加入一定量的含碘(I2)2.54mg的碘溶液,再加入2~3滴淀粉溶液(I2遇淀粉溶液显示蓝色),通过抽气装置抽气,使空气由导气管进入试管与碘溶液充分接触,当溶液由蓝色变为无色时,恰好完全反应.反应的化学方程式是:SO2+I2+2H2O→H2SO4+2HI.实验过程中进入试管内的空气的总体积为1500L.请通过计算判断出此空气中二氧化硫的浓度级别.
 二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:
二氧化硫是大气污染物之一.我国的环境空气质量标准中对空气中二氧化硫的最高浓度(单位体积的空气中所含二氧化硫的质量)限值如下表所示:| 浓度限值(mg/m3) | ||
| 一级指标 | 二级指标 | 三级指标 |
| 0.15 | 0.50 | 0.70 |
17.成语是中华文化的精粹,下列成语中存在化学变化的是( )
| A. | 鸡飞蛋打 | B. | 拔苗助长 | C. | 滴水石穿 | D. | 灰飞烟灭 |
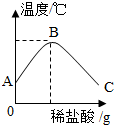 将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸质量的变化如图所示.由图可知,稀盐酸与氢氧化钠溶液发生的反应是放热(填“放热”或“吸热”)反应,从A到B过程中,烧杯中溶液的pH变化是逐渐减小,B点表示的含义是稀盐酸和氢氧化钠恰好完全反应,此时溶液中的主要微粒有Na+ Cl-H2O(写微粒符号).
将稀盐酸慢慢滴入装有氢氧化钠溶液的烧杯中,用温度计测出烧杯中溶液的温度,溶液温度随加入稀盐酸质量的变化如图所示.由图可知,稀盐酸与氢氧化钠溶液发生的反应是放热(填“放热”或“吸热”)反应,从A到B过程中,烧杯中溶液的pH变化是逐渐减小,B点表示的含义是稀盐酸和氢氧化钠恰好完全反应,此时溶液中的主要微粒有Na+ Cl-H2O(写微粒符号).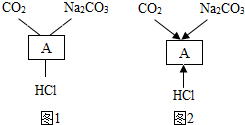 请根据物质化学性质知识网络图回答问题.(“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.)
请根据物质化学性质知识网络图回答问题.(“-”表示相连的两种物质能发生反应,“→”表示一种物质转化成另一种物质.)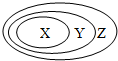 如图表示物质类别的从属关系图,如表所示的物质类别不能满足如图关系的是( )
如图表示物质类别的从属关系图,如表所示的物质类别不能满足如图关系的是( )