题目内容
2.请分析下列实验或事实,分别说明在其他条件不变时,这些因素是如何影响化学反应.示例:硫在纯氧中燃烧比在空气中进行得更快,更剧烈.答增大反应物浓度,可以加快化学反应速率.(1)粉末块的石灰石比相同质量的块状的石灰石与相同的盐酸反应更快;
(2)碳在氧气充足时生成二氧化碳,氧气不足时产生一氧化碳.
分析 影响化学反应的因素有:温度,温度越高,反应越快;反应物的接触面积,物质间的接触面积越充分,反应速度越快;反应物颗粒的大小,颗粒越小,反应速度越快;通常反应物的浓度越大,反应速度越快;加入催化剂可以改变其反应速率等;据此结合事实进行分析解答.
解答 解:(1)粉末块的石灰石比相同质量的块状的石灰石与相同的盐酸反应更快,粉末块的石灰石与稀盐酸的接触面积答,增大接触面积,反应速率加快,
(2)碳在氧气充足时生成二氧化碳,氧气不足时产生一氧化碳,是因为反应物的量不同,生成物可能不同.
故答案为:(1)增大接触面积,反应速率加快;(2)反应物的量不同,生成物可能不同.
点评 本题难度不是很大,了解影响化学反应的因素即可正确解答本题,可从温度、反应物的接触面积、反应物颗粒的大小、反应物的浓度及催化剂等方面进行分析考虑.

练习册系列答案
相关题目
12.现有镁和另一种金属组成的混合物,取2.4g该混合物加入100g一定溶质质量分数的稀硫酸,两者恰好完全反应,产生氢气的质量为a,下列说法正确的是( )
| A. | 若混合物为Mg、Al,a可能是0.2g | |
| B. | 若混合物为Mg、Fe,a不可能是0.2g | |
| C. | 若混合物为Mg、Zn,a可能是0.1g,则该混合物中镁的质量分数为50% | |
| D. | 若混合物为Mg、Al,则稀硫酸中溶质质量分数一定大于9.8% |
7.如图所示物品所使用的主要材料属于合金的是( )
| A. |  橡胶轮胎 | B. |  木雕作品 | C. |  艺术瓷瓶 | D. |  青铜摆件 |
14.下列实验操作错误的是( )
| A. |  | B. | 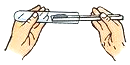 | C. | 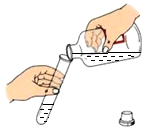 | D. |  |
11.下列关于S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2的说法不正确的是( )
| A. | 参加反应的硫与氧气的质量比为2:1 | |
| B. | 表示硫与氧气在点燃条件下反应生成二氧化硫 | |
| C. | 反应前后硫原子、氧原子的个数均不变 | |
| D. | 参加反应的氧气与生成的二氧化硫的分子个数比为1:1 |
12.下列关于实验操作或实验现象的描述错误的是( )
| A. | 实验剩余的药品不能放回原瓶,应放到指定容器中 | |
| B. | 稀释浓硫酸时要把浓硫酸缓缓注入水中,并用玻璃棒不断搅拌 | |
| C. | 将pH试纸放入待测液中,测定溶液的pH | |
| D. | 加热高锰酸钾制取氧气,实验开始时应先检查装置的气密性,确保装置不漏气 |
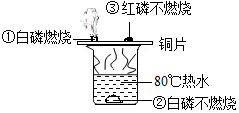 如图是有关探究燃烧条件的实验现象,请你判断下列各说法的正误(用“√”、“×”标出)
如图是有关探究燃烧条件的实验现象,请你判断下列各说法的正误(用“√”、“×”标出) 如图所示,是测定白磷燃烧前后质量变化情况,用来验证质量守恒定律的实验,试回答:
如图所示,是测定白磷燃烧前后质量变化情况,用来验证质量守恒定律的实验,试回答: